
下列说法正确的是
①经分析某物质只含有一种元素,则该物质一定是单质;
②根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等;
③NO2和水反应能生成硝酸,但NO2不是酸性氧化物
④溶液是电中性的,胶体是带电的
⑤不能发生丁达尔效应的分散系有氯化钠溶液、水等
A.①③④ B.仅③ C.仅⑤ D.②③④⑤
科目:高中化学 来源: 题型:
有浓度为0.1 mol•L-1的盐酸、硫酸、醋酸三种溶液,试回答:
(1) 三种溶液中c(H+) 依次为a mol•L-1,b mol•L-1,c mol•L-1,大小顺序为______。
(2)等体积的以上三种酸分别与过量的NaOH 溶液反应,生成的盐的物质的量依次为n 1mol,n2 mol,n3 mol,它们的大小关系为____________。
(3)中和等量NaOH溶液都生成正盐时,分别需上述三种酸的体积依次是V1L、V2L、V3L,其大小关系为___________________________________________。
(4)与等量锌反应时产生氢(气)的速率分别为v1、v2、v3,其大小关系为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1
2H2(g)+O2(g)═2H2O(g)△H2
C(s)+O2(g)═CO2(g)△H3
则反应4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为( )
|
| A. | 12△H3+5△H2﹣2△H1 | B. | 2△H1﹣5△H2﹣12△H3 | C. | 12△H3﹣5△H2﹣2△H1 | D. | △H1﹣5△H2﹣12△H3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
现将1mo1Cu2S与144克FeO投入到足量稀硝酸溶液中,充分反应得到Fe(NO3)3、Cu(NO3)2 、CuSO4的混合溶液,并产生NO气体。则最终反应所得NO物质的量为
A.4 mo1 B.5 mo1 C.6 mo1 D.7 mo1
查看答案和解析>>
科目:高中化学 来源: 题型:
HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________(填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是________(填序号)。
A.测定这两种溶液的pH  B.分别在两种溶液中滴加甲基橙
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别 D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:________________________ 。
(4) Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________(填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.目前使用的元素周期表中,最长的周期含有36种元素.
B.周期表中所有元素都是从自然界中发现的,过渡元素都是金属元素
C.非金属元素形成的共价化合物中,原子的最外层电子数只能是2或8
D.IA族与VIIA族元素间可形成共价化合物或离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
用铝制易拉罐收集满CO2,快速加入过量NaOH浓溶液,立即把口封闭。发现易拉罐“咔咔”作响,并变瘪了:过一会儿,易拉罐又会作响并鼓起来。下列说法正确的是
A.导致易拉罐变瘪的离子反应是:CO2+OH-═HCO3-
B.导致易拉罐又鼓起来的反应是: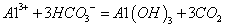
C.若将CO2换为NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象
D.上述过程中与NaOH溶液反应的物质有三种,且反应结束后的溶液显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列装置能达到预期目的的是( )
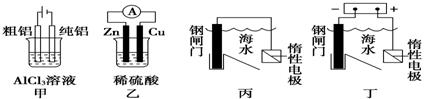
A.甲图装置可用于电解精炼铝 B.乙图装置可得到持续、稳定的电流
C.丙图装置可达到保护钢闸门的目的 D.丁图装置可达到保护钢闸门的目的
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需要 0.1mol/L的 H2SO4溶液980mL,欲用 98%、密度为1.84g/cm3的浓硫酸配制.
(1)所需的主要仪器除量筒、烧杯、玻璃棒外,还需要 、 。
(2)其实验操作步骤可分为以下几步:
A.用量筒量取 mL浓硫酸,缓缓注入装有约50mL蒸馏水的烧杯里,并用玻璃棒搅拌。
B.用适量蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液都移入容量瓶里。
C.将稀释后的硫酸小心地用玻璃棒引流容量瓶里。
D.检查容量瓶是否漏水。
E.将蒸馏水直接加入容量瓶,至液面接近刻度线1-2cm处。
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液。
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻线相切。
请据此填写:
①完成上述步骤中的空白处。
②补充完成正确的操作顺序(用字母填写):
( D )→( A )→( C )→( )→( )→( )→( F )。
③将浓硫酸在烧杯中稀释后移入容量瓶时,必须_________________方可移液.
(3)试分析下列操作对所配溶液的浓度有何影响
①量取浓硫酸时眼睛俯视量筒刻度线,会导致所配溶液浓度会 ;(填: 偏高、偏低、或无影响,下同)
②定容时,眼睛仰视刻度线,所配溶液浓度会 ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com