
 硫酸亚铁铵[(NH4)2Fe(SO4)2•6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁.硫酸亚铁铵在 500℃时隔绝空气加热完全分解.回答下列问题:
硫酸亚铁铵[(NH4)2Fe(SO4)2•6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁.硫酸亚铁铵在 500℃时隔绝空气加热完全分解.回答下列问题:分析 (1)氮元素和铁元素化合价升高,根据在氧化还原反应中化合价有升必有降,化合价降低的应该是硫,所以气体产物中还可能有SO2;
(2)①A中固体充分加热较长时间后,通入氮气目的是使分解生成的气体在BC装置中完全吸收;
②为验证A中残留物是否含有FeO,应该先用稀硫酸溶解,然后再用KMnO4溶液检验亚铁离子;
③装置B中BaC12溶液的作用是为了检验分解产物中是否有SO3气体生成,若含有该气体,会生成硫酸钡白色沉淀,观察到的观象为溶液变浑浊;
④若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为bmol,C中沉淀物质的量为amol,根据化合价升降必相等,硫降低的化合价(2a)等于铁升高的化合价(2b)和氮升高的化合价之和,则b小于a;
⑤C中有白色沉淀生成,是因为SO2被双氧水氧化成SO42-,SO42-再与Ba2+结合成沉淀BaSO4,则C中发生的反应为SO2+H2O2+Ba2+=BaSO4↓+2H+;
(3)硫酸亚铁铵溶液较硫酸亚铁溶液不易被氧气氧化是因为溶液中铵根离子水解显酸性,氢离子浓度增大,抑制氧化还原反应的发生.
解答 解:(1)氮元素和铁元素化合价升高,根据在氧化还原反应中化合价有升必有降,化合价降低的应该是硫,所以气体产物中还可能有SO2,故答案为:SO2;
(2)①A中固体充分加热较长时间后,通入氮气目的是使分解生成的气体在BC装置中完全吸收,故答案为:使分解产生的气体在B、C中被吸收充分;
②为验证A中残留物是否含有FeO,应该先用稀硫酸溶解,然后再用KMnO4溶液检验亚铁离子,故选BD,
故答案为:BD;
③装置B中BaC12溶液的作用是为了检验分解产物中是否有SO3气体生成,若含有该气体,会生成硫酸钡白色沉淀,观察到的观象为溶液变浑浊;
故答案为:SO3;溶液变浑浊;
④若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为bmol,C中沉淀物质的量为amol,根据化合价升降必相等,硫降低的化合价(2a)等于铁升高的化合价(2b)和氮升高的化合价之和,则b小于a,
故答案为:小于;
⑤C中有白色沉淀生成,是因为SO2被双氧水氧化成SO42-,SO42-再与Ba2+结合成沉淀BaSO4,则C中发生的反应为SO2+H2O2+Ba2+=BaSO4↓+2H+,
故答案为:SO2+H2O2+Ba2+=BaSO4↓+2H+;
(3)硫酸亚铁铵溶液较硫酸亚铁溶液不易被氧气氧化是因为溶液中铵根离子水解显酸性,氢离子浓度增大,抑制氧化还原反应的发生,
故答案为:硫酸亚铁铵溶液中NH4+发生水解增大c(H+),抑制了上述氧化还原反应的进行.
点评 本题考查了物质性质的实验探究和实验设计,注意氧化还原反应和盐类水解等知识的灵活应用,题目难度中等.


科目:高中化学 来源: 题型:解答题
 前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2.
前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2. ,很多不饱和有机物在E催化下可与H2发生加成反应:如①CH2=CH2、②HC≡CH、③$\sqrt{2}$、④HCHO.其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角 形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质)加成产物CH3OH分子之间能形成氢键.
,很多不饱和有机物在E催化下可与H2发生加成反应:如①CH2=CH2、②HC≡CH、③$\sqrt{2}$、④HCHO.其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角 形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质)加成产物CH3OH分子之间能形成氢键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  如图研究的是温度、压强对平衡的影响,横坐标表示压强 | |
| B. | 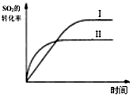 如图研究的是温度对平衡的影响,Ⅱ采用的温度更高 | |
| C. | 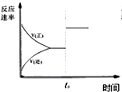 图中t0时使用了催化剂,使平衡向正反应方向进行 | |
| D. | 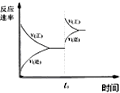 图中t0时增大压强,使平衡向负反应方向进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玉是石灰石 | B. | 玉的硬度比河砂大 | ||
| C. | 玉的熔点较高 | D. | 玉是金刚砂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
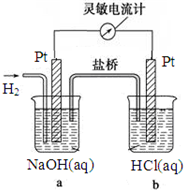 如图向a中通入H2,发现灵敏电流计指针发生偏转,持续通入H2可观察到b中铂电极表面有少量气泡产生,负极反应式为H2-2e-+2OH-=2H2O,电池的总反应为HCl+NaOH=H2O+NaCl.
如图向a中通入H2,发现灵敏电流计指针发生偏转,持续通入H2可观察到b中铂电极表面有少量气泡产生,负极反应式为H2-2e-+2OH-=2H2O,电池的总反应为HCl+NaOH=H2O+NaCl.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫原子结构示意图: | |
| B. | 氯化氢分子的电子式: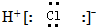 | |
| C. | 乙烯分子的结构式:CH2=CH2 | |
| D. | 硫酸铁的电离方程式:Fe2(SO4)3=2 Fe3++3SO42ˉ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温度、容积不变,充入NH3 | B. | 温度、容积不变时,充入SO2气体 | ||
| C. | 充入N2,保持压强不变 | D. | 移走一部分NH4HS固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com