
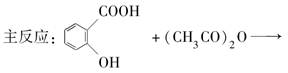
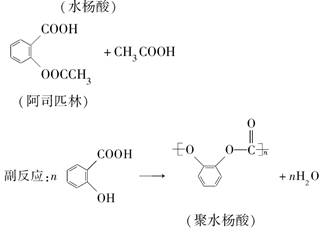
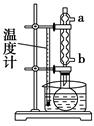
科目:高中化学 来源:不详 题型:单选题
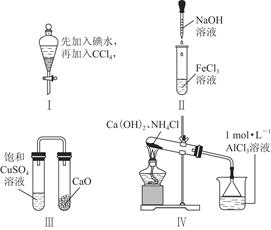
| A.实验Ⅰ:振荡后静置,液体分层,下层液体无色 |
| B.实验Ⅱ:滴入氢氧化钠溶液后,试管中出现白色沉淀,白色沉淀迅速变为灰绿色,最后变为红褐色 |
| C.实验Ⅲ:一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
| D.实验Ⅳ:加热后,水槽中先生成白色沉淀,后逐渐溶解 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
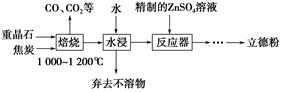
 BaS(s)+4CO2(g),该反应的平衡常数的表达式为__________________________________________________。
BaS(s)+4CO2(g),该反应的平衡常数的表达式为__________________________________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 物质 | 杂质 | 试剂 | 主要操作 |
| A | NaHCO3固体 | Na2CO3固体 | / | 加热 |
| B | SiO2 | Fe2O3 | 盐酸 | 过滤 |
| C | KBr溶液 | Br2 | KOH溶液 | 分液 |
| D | Cl2 | HCl | 饱和碳酸钠溶液 | 洗气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.肯定有Al3+、SO42-,可能有K+、NH4+ |
| B.肯定无NH4+、Mg2+、CO32-,可能有Fe2+ |
| C.原溶液一定是明矾和MgSO4的混合溶液 |
| D.肯定有Mg2+,K+只能通过焰色反应才能确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
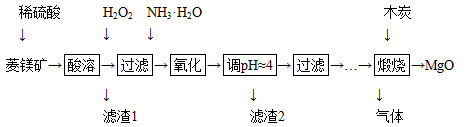
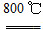 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑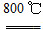 MgO+SO2↑+CO↑
MgO+SO2↑+CO↑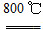 MgO+S↑+3CO↑
MgO+S↑+3CO↑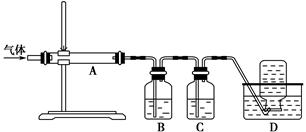
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 混合物 | 试剂 | 分离方法 |
| A | Fe(碘) | — | 加热 |
| B | 二氧化碳(氯化氢) | 饱和Na2CO3溶液 | 洗气 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| D | 淀粉(氯化钠) | 蒸馏水 | 渗析 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
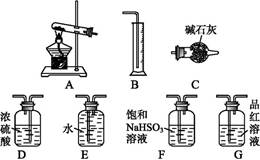
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.过滤 | B.蒸发 | C.蒸馏 | D.萃取 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com