
| A. | 离子结构示意图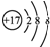 :可以表示35Cl-,也可以表示37Cl- :可以表示35Cl-,也可以表示37Cl- | |
| B. | 电子式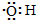 :可以表示羟基,也可以表示氢氧根离子 :可以表示羟基,也可以表示氢氧根离子 | |
| C. | 比例模型 :可以表示甲烷分子,也可以表示四氯化碳分子 :可以表示甲烷分子,也可以表示四氯化碳分子 | |
| D. | 聚丙烯的结构简式: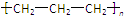 |
分析 A.35Cl-和37Cl-;是同种元素,质子数相同电子数也相同,所以离子结构示意图相同;
B.氢氧根离子带一个单位的负电荷;
C.Cl原子半径大于C原子,比例模型不正确;
D.聚丙烯的结构单元的主链含有2个C原子.
解答 解:A.35Cl-和37Cl-;是同种元素,质子数相同电子数也相同,所以离子结构示意图相同,故A正确;
B.氢氧根离子的电子式为: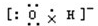 ,羟基的电子式为
,羟基的电子式为 ,故B错误;
,故B错误;
C.Cl原子半径大于C原子,四氯化碳分子比例模型不正确,比例模型应符合原子的大小,故C错误;
D.聚丙烯为丙烯通过加聚反应生成的,聚丙烯的结构简式为: ,故D错误;
,故D错误;
故选A.
点评 本题考查离子结构示意图,电子式,比例模型、有机物结构简式等,掌握电子式、结构简式等化学用语的概念及正确的表示方法是解题管就,题目难度不大.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | B. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | ||
| C. | C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2 | D. | C+CO2$\frac{\underline{\;\;△\;\;}}{\;}$2CO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝的熔点很高,可用于制作耐高温材料 | |
| B. | Na2O2能与水和二氧化碳反应生成氧气,可用于呼吸面具中作为氧气的来源 | |
| C. | 明矾能在天然水中生成Al(OH)3胶体,可用作净水剂 | |
| D. | 用氢氟酸雕刻玻璃,是由于氢氟酸能与二氧化硅反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在0.01mol•L-1Ba(OH)2溶液中:Na+、NH4+、NO3-、HCO3- | |
| B. | 使甲基橙变红色的溶液中:Mg2+、Fe2+、NO3-、Cl- | |
| C. | pH=7的溶液中:K+、Cl-、Br-、Fe3+ | |
| D. | 水电离的c(H+)=1×10-13mol•L-1的溶液中:K+、Na+、I-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
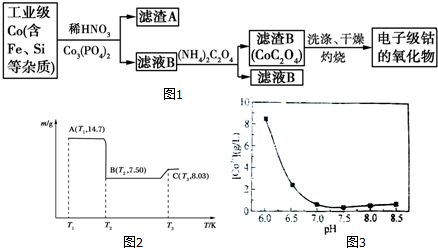
| 开始沉淀的pH | 完全沉淀的pH | |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Co2+ | 7.2 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①③⑥ | C. | ②③④ | D. | ①④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
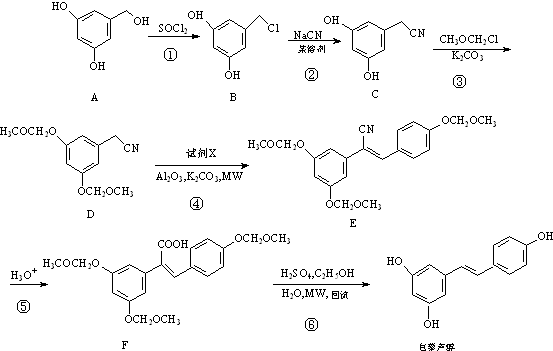
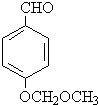 .
.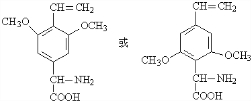 .
.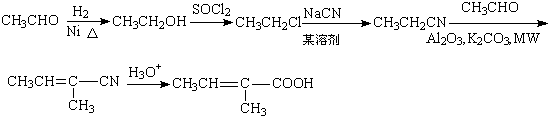 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com