
下列叙述正确的是( )
A.同周期元素中ⅦA族元素的相对原子质量最大
B.ⅥA族元素的原子,其半径越大,越容易得到电子
C.同周期中ⅠA族元素的金属性比ⅡA族元素的金属性强
D.所有主族元素的原子,形成单原子离子时的化合价和它的族序数相等
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
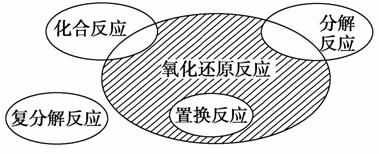
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影部分的是 ( )。
A.Cl2+2KBr===Br2+2KCl
B.2NaHCO3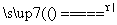 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O===4Fe(OH)3
D.2Na2O2+2CO2===2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
某市晚报曾报道,该市七条交通主干道的空气污染严重,其主要原因是
( )。
A.燃烧煤所排放的废气造成的
B.几十万辆汽车、助力车等排放的废气造成的
C.工业生产中的废渣、废水、废气造成的
D.不断地降雨和各种污水造成的
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两烧杯中分别装有相同pH的氨水和NaOH溶液,各加入10 mL
0.1 mol·L-1AlCl3溶液,两烧杯中都有沉淀生成。下列判断正确的是( )
A.甲中沉淀一定比乙中的多
B.甲中沉淀可能比乙中少
C.甲和乙中反应的离子方程式相同
D.甲和乙中的沉淀不可能一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| T | M层上电子数是K层上的电子数的3倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(1)X的原子结构示意图为________。
(2)元素Y与氢元素形成一种离子YH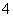 ,写出该微粒的电子式________(用元素符号表示)。
,写出该微粒的电子式________(用元素符号表示)。
(3)元素Z与元素T相比,非金属性较强的是______(用元素符号表示),下列表述中能证明这一事实的是________。
a.常温下Z的单质和T的单质状态不同
b. Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是(写出该种元素的最高价氧化物的水化物的化学式)________,理由是__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
反应2SO2(g)+O2(g)2SO3(g)经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为( )
A.0.1 s B.2.5 s
C.5 s D.10 s
查看答案和解析>>
科目:高中化学 来源: 题型:
对无机化合物可根据其组成和性质进行如下分类:

(1)如图所示的物质分类方法可称为树状分类法.
(2)以Na、H、C、N、O、S、Cl等元素中任选两种或三种元素组成合适的一种物质,将其化学式分别填在下表中的相应位置.
物质
类别 酸 碱 盐 氧化物
化学式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com