
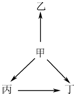
 下列各组物质中,物质之间通过一步反应就能实现如图所示变化的是( )
下列各组物质中,物质之间通过一步反应就能实现如图所示变化的是( )| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | N2 | NH3 | NO | NO2 |
| B | Na | Na2O | NaOH | Na2O2 |
| C | SiO2 | SiF4 | H2SiO3 | Na2SiO3 |
| D | Al | AlCl3 | Al2O3 | NaAlO2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、氮气转化为二氧化氮,要两步进行氮气放电生成一氧化氮,一氧化氮再被氧化生成二氧化氮;
B、氢氧化钠无法转化过氧化钠;
C、SiO2无法一步转化为H2SiO3;
D、甲→乙:Al$\stackrel{氯气}{→}$AlCl3;甲→丙:Al$\stackrel{氧气}{→}$Al2O3;甲→丁:Al$\stackrel{过量的氢氧化钠}{→}$NaAlO2;丙→丁:Al2O3$\stackrel{过量的氢氧化钠}{→}$NaAlO2.
解答 解:A、氮气转化为二氧化氮,要两步进行氮气放电生成一氧化氮,一氧化氮再被氧化生成二氧化氮,不实现甲到丁的一步转化,故A错误;
B、氢氧化钠无法转化过氧化钠,故B错误;
C、SiO2无法一步转化为H2SiO3,首先二氧硅与强碱反应生成硅酸盐,然后再利用强制弱生成硅酸,故C错误;
D、甲→乙:Al$\stackrel{氯气}{→}$AlCl3;甲→丙:Al$\stackrel{氧气}{→}$Al2O3;甲→丁:Al$\stackrel{过量的氢氧化钠}{→}$NaAlO2;丙→丁:Al2O3$\stackrel{过量的氢氧化钠}{→}$NaAlO2,各步都可以实现一步转化,故D正确;
故选D.
点评 本题考查无机物的推断,明确各物质的性质来分析转化发生的反应是解答本题的关键,注意某些转化中的答案是不唯一的,题目难度中等.


科目:高中化学 来源: 题型:选择题
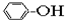 ⑥
⑥ ⑦
⑦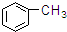 ⑧
⑧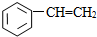
| A. | ①③ | B. | ②④ | C. | ⑤⑥ | D. | ⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
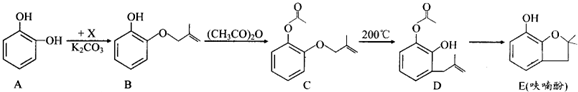
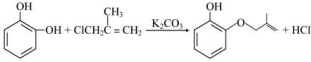 ;
; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
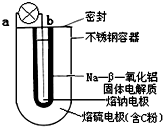 钠-硫($\frac{Na}{{S}_{8}}$)电池是由固体电解质将两个液体电极隔开(如图),一个由钠-β-氧化铝固体电解质做成的中心管,将内室的熔融钠(熔点98℃)和外室的熔融硫(熔点119℃)隔开,并允许Na+通过.下列有关说法错误的是( )
钠-硫($\frac{Na}{{S}_{8}}$)电池是由固体电解质将两个液体电极隔开(如图),一个由钠-β-氧化铝固体电解质做成的中心管,将内室的熔融钠(熔点98℃)和外室的熔融硫(熔点119℃)隔开,并允许Na+通过.下列有关说法错误的是( )| A. | 放电时b为电池的负极 | |
| B. | 充电时阴极反应式为:Na++e-=Na | |
| C. | 充电时,阳极处发生还原反应 | |
| D. | 放电时Na+可以穿过固体电解质流向a电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨汽化时吸收大量的热,可用作制冷剂 | |
| B. | 硅酸钠溶液呈碱性,可用作木材防火剂 | |
| C. | NaHCO3能与碱反应,可用作焙制糕点的膨松剂 | |
| D. | Fe比Cu活泼,可用FeCl3溶液腐蚀线路板上的Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 常温下0.1 mol•L-1的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,c(N${{H}_{4}}^{+}$)由大到小的顺序为②>①>③ | |
| B. | 常温下0.4 mol•L-1CH3COOH溶液和0.2 mol•L-1 NaOH溶液等体积混合后溶液显酸性,则溶液中粒子浓度由大到小的顺序为c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) | |
| C. | 0.1 mol•L-1 Na2CO3溶液与0.2 mol•L-1 NaHCO3溶液等体积混合所得溶液中:c(C${{O}_{3}}^{2-}$)+2c(OH-)=c(HC${{O}_{3}}^{-}$)+3c(H2CO3)+2c(H+) | |
| D. | 0.1 mol•L-1的氨水与0.05 mol•L-1 H2C2O4溶液等体积混合所得溶液中:c(N${{H}_{4}}^{+}$)+c(NH3•H2O)=2c(C2${{O}_{4}}^{2-}$)+2c(HC2${{O}_{4}}^{-}$)+2c(H2C2O4) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径的大小顺序:r(W)>r(Z)>r(Y) | |
| B. | 元素Z、M的简单离子的电子层结构相同 | |
| C. | W的简单气态氢化物的热稳定性比M的差 | |
| D. | 元素X和Y形成的化合物只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 操作步骤 | 现象 |
| 步骤1:向2mL 0.005mol•L-1 AgNO3溶液中加入2mL 0.005mol•L-1KSCN溶液,静置. | 出现白色沉淀. |
| 步骤2:取1mL上层清液于试管中,滴加1滴2mol•L-1 Fe(NO3)3溶液. | 溶液变红色. |
| 步骤3:向步骤2的溶液中,继续加入5滴3mol•L-1AgNO3溶液. | 出现白色沉淀,溶液红色变浅. |
| 步骤4:向步骤1余下的浊液中加入5滴3mol•L-1KI溶液. | 出现黄色沉淀. |
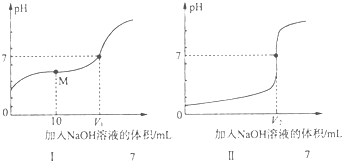
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
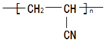 路线:
路线:
 .
.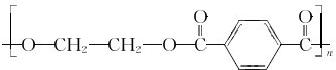 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com