
( 16分)活性ZnO俗称锌1-3,能改逬玻璃的化学稳定性,可用于生产特种玻璃,在橡胶的虫产屮能缩短硫化吋间,在涂料、油漆等工业也有重要应用。工业上由粗ZnO(含FeO、CuO等.)制备活性ZnO,采取酸浸、净化除杂、中和沉降、干燥煅烧等步骤,工艺流程如下: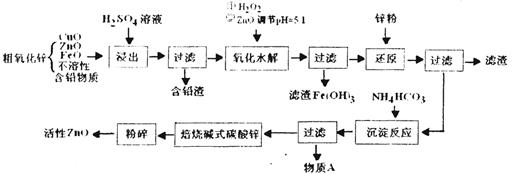
(1 )上述流程屮,浸出用的是60%H2SO4(1.5g/cm3),这种硫酸的物质的量浓度为________(保留两位小数)
(2 )已知ZnO为两性氧化物,与氢氧化钠溶液反应生成可溶性的锌酸盐(Zn02-),写出反应的离子方程式________________
(3) 写出加H2O2吋发生反应的离子方程式________________
(4) 除去Fe(OH)3后,在滤液中加入Zn的目的是________
(5) 上述流程中多次进行了过滤橾作,请写出过滤时用到的玻璃仪器:________________
(6) 物质A是________,检验该溶质阴离子的方法是________
(7) 取碱式碳酸锌6.82g,溶于盐酸生成C02 448mL(标准状况下),溶解过程消耗HCl 0. 12mol,若该碱式盐中氢元素的质量分数为1.76%,试推测该碱式碳酸锌的化学式________
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2010-2011学年安徽省合肥市高三第二次教学质量检测理综化学部分 题型:填空题
( 16分)活性ZnO俗称锌1-3,能改逬玻璃的化学稳定性,可用于生产特种玻璃,在橡胶的虫产屮能缩短硫化吋间,在涂料、油漆等工业也有重要应用。工业上由粗ZnO(含FeO、CuO等.)制备活性ZnO,采取酸浸、净化除杂、中和沉降、干燥煅烧等步骤,工艺流程如下:

(1 )上述流程屮,浸出用的是60%H2SO4(1.5g/cm3),这种硫酸的物质的量浓度为________(保留两位小数)
(2 )已知ZnO为两性氧化物,与氢氧化钠溶液反应生成可溶性的锌酸盐(Zn02-),写出反应的离子方程式________________
(3) 写出加H2O2吋发生反应的离子方程式________________
(4) 除去Fe(OH)3后,在滤液中加入Zn的目的是________
(5) 上述流程中多次进行了过滤橾作,请写出过滤时用到的玻璃仪器:________________
(6) 物质A是________,检验该溶质阴离子的方法是________
(7) 取碱式碳酸锌6.82g,溶于盐酸生成C02 448mL(标准状况下),溶解过程消耗HCl 0. 12mol,若该碱式盐中氢元素的质量分数为1.76%,试推测该碱式碳酸锌的化学式________
查看答案和解析>>
科目:高中化学 来源: 题型:
( 16分)活性ZnO俗称锌1-3,能改逬玻璃的化学稳定性,可用于生产特种玻璃,在橡胶的虫产屮能缩短硫化吋间,在涂料、油漆等工业也有重要应用。工业上由粗ZnO(含FeO、CuO等.)制备活性ZnO,采取酸浸、净化除杂、中和沉降、干燥煅烧等步骤,工艺流程如下:
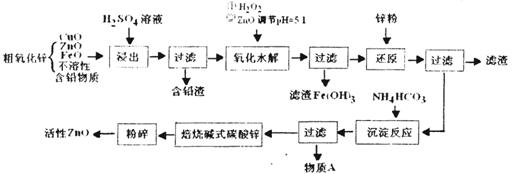
(1 )上述流程屮,浸出用的是60%H2SO4(1.5g/cm3),这种硫酸的物质的量浓度为________(保留两位小数)
(2 )已知ZnO为两性氧化物,与氢氧化钠溶液反应生成可溶性的锌酸盐(Zn02-),写出反应的离子方程式________________
(3) 写出加H2O2吋发生反应的离子方程式________________
(4) 除去Fe(OH)3后,在滤液中加入Zn的目的是________
(5) 上述流程中多次进行了过滤橾作,请写出过滤时用到的玻璃仪器:________________
(6) 物质A是________,检验该溶质阴离子的方法是________
(7) 取碱式碳酸锌6.82g,溶于盐酸生成C02 448mL(标准状况下),溶解过程消耗HCl 0. 12mol,若该碱式盐中氢元素的质量分数为1.76%,试推测该碱式碳酸锌的化学式________
查看答案和解析>>
科目:高中化学 来源: 题型:
( 16分)活性ZnO俗称锌1-3,能改逬玻璃的化学稳定性,可用于生产特种玻璃,在橡胶的虫产屮能缩短硫化吋间,在涂料、油漆等工业也有重要应用。工业上由粗ZnO(含FeO、CuO等.)制备活性ZnO,采取酸浸、净化除杂、中和沉降、干燥煅烧等步骤,工艺流程如下:
(1 )上述流程屮,浸出用的是60%H2SO4(1.5g/cm3),这种硫酸的物质的量浓度为________(保留两位小数)
(2 )已知ZnO为两性氧化物,与氢氧化钠溶液反应生成可溶性的锌酸盐(Zn02-),写出反应的离子方程式________________
(3) 写出加H2O2吋发生反应的离子方程式________________
(4) 除去Fe(OH)3后,在滤液中加入Zn的目的是________
(5) 上述流程中多次进行了过滤橾作,请写出过滤时用到的玻璃仪器:________________
(6) 物质A是________,检验该溶质阴离子的方法是________
(7) 取碱式碳酸锌6.82g,溶于盐酸生成C02448mL(标准状况下),溶解过程消耗HCl 0. 12mol,若该碱式盐中氢元素的质量分数为1.76%,试推测该碱式碳酸锌的化学式________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com