
某课外实验小组设计的下列实验不合理的是( )

A.图1:蒸干NH4Cl饱和溶液制备NH4Cl晶体
B.图2:实验室制备少量氨气
C.图3:制备并观察氢氧化亚铁
D.图4:证明过氧化钠与水反应放热
科目:高中化学 来源: 题型:
下列有关元素周期表、元素周期律的说法中正确的是
①所有元素的最高化合价都等于元素原子的最外层电子数
②最外层一个电子的元素一定是金属元素,肯定在元素周期表的第IA族
③ⅡA族中无非金属元素
④第3周期元素随原子序数增大各非金属元素对应的氧化物的水化物酸性一定逐渐增强
⑤同主族元素随原子序数增大,其原子半径逐渐增大
⑥ 副族元素中没有非金属元素,元素周期表中金属元素的种类比非金属元素多
A. ①②③④⑤⑥ B. ①②③⑥ C.③④⑤ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
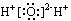 A.H2O的电子式: B.质量数为14的碳原子:
A.H2O的电子式: B.质量数为14的碳原子: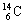
C.CO2的比例模型: D.Cl-的结构示意图:
D.Cl-的结构示意图:
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生为了探究Zn与盐酸反应过程中的速率变化,在100mL稀盐酸中加入足量的Zn粉,用排水集气法收集反应放出的H2,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标况下) | 50 | 120 | 232 | 290 | 310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大 ,你认为原因是 。
(2)4~5 min时间段的反应速率最小,你认为原因是 。
(3)求2~3 min时间段内以盐酸的浓度变化来表示的反应速率(假设溶液体积保持不变)V(HCl)= 。
(4)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入下列物质:
A.H2O B.NaCl溶液 C.Na2CO3溶液 D.Cu粉 E.CuSO4粉末
你认为可行的是(填编号) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z是周期表中相邻的三种短周期元素,它们原子半径依次减小,X与Z的核电荷数之比为3∶4,X、Y、Z分别与氢元素形成氢化物。下列叙述正确的是( )
A.Z是第二周期IVA族元素 B.最高价氧化物对应的水化物的酸性: Y﹥X
C.非金属性:X﹥Y﹥Z D.X、Y、Z的氢化物稳定性逐渐减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
7下列说法正确的是( )
A.自然界中含有大量的游离态的硅,纯净的硅晶体可用于制作计算机芯片
B.Si、P、S、Cl 相应的最高价氧化物对应水化物的酸性依次增强
C.工业上通常用电解钠、铁、铜对应的氯化物制得该三种金属单质
D.金属铝、铁、铜都有一定的抗腐蚀性能,其抗腐蚀的原因都是表面形成氧化物薄膜,阻 止反应的进一步进行
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z是3种短周期元素,其中X、Y位于同一族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是( )
A.元素非金属性由弱到强的顺序为Z<Y<X
B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4
C.3种元素的气态氢化物中Z的气态氢化物最稳定
D.原子半径由大到小的顺序为Z<Y<X
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室常用苯甲醛在浓氢氧化钠溶液中制备苯甲醇和苯甲酸。
已知:
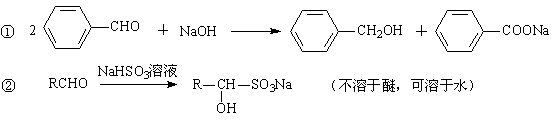
③苯甲酸易溶于乙醇,微溶于冷水,可溶于热水。
④乙醚沸点34.6℃,密度0.7138,易燃烧。当空气中含量为1.83~48.0%时易发生爆炸。
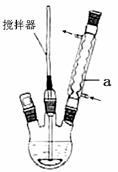 主要实验装置和步骤如下:
主要实验装置和步骤如下:
Ⅰ.向如图所示装置中加入8g氢氧化钠和30mL水,搅拌溶解,稍冷后
加入10 mL苯甲醛。在搅拌下反应40 min后,停止加热,从仪器a
上口加入冷水20 mL,冷却至室温。
Ⅱ.用乙醚萃取并分液。水层保留待用。醚层依次用少量饱和亚硫酸氢钠
溶液和蒸馏水洗涤后,分出醚层,倒入干燥的锥形瓶,加无水硫酸镁
干燥,注意锥形瓶上要加塞。将锥形瓶中溶液转入蒸馏装置,加热蒸出
乙醚;再升高温度,收集198℃~204℃的馏分得产品A。
Ⅲ.将步骤Ⅱ萃取后备用的水层慢慢地加入到盛有30 mL浓盐酸和30 mL水
的混合物中,同时用玻璃棒搅拌,析出白色固体。冷却,抽滤,得到粗
产品,然后提纯得产品B。
根据以上步骤回答下列问题:
(1)写出玻璃仪器a的名称 ;其作用是 。
(2)步骤Ⅱ萃取时用到的玻璃仪器除了烧杯、玻璃棒外,还需 ,饱和亚硫酸氢钠溶液洗涤的目的是 ,
(3)产品A为 ,蒸馏除乙醚的过程中采用的加热方式为 。
(4)步骤Ⅱ用无水硫酸镁干燥时需要在锥形瓶上加塞,其原因是 。
(5)抽滤过程中需要洗涤产品晶体,下列液体最适合的是_______。
A.无水乙醇 B.饱和NaHCO3溶液 C.冷水 D.滤液
(6)停止抽滤的操作方法是 。提纯B的粗产品的实验操作名称为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com