
将Mg条投入盛有稀HCl的容器里,产生H2的速率与下列因素:
①盐酸浓度 ②温度 ③镁条的表面积 ④溶液中c(Cl-)大小,有关系的是
A.①② B.③④ C.①②③ D.①②③④
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届福建省高三上学期半期考试化学试卷(解析版) 题型:填空题
(8分)
某化学兴趣小组用以下装置探究SO2的某些化学性质。
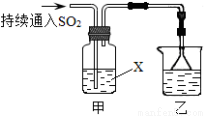
(1)装置乙的作用是 。
(2)若X为品红溶液,观察到溶液褪色,说明SO2具有 (填序号,下同);若X为Na2S溶液,观察到溶液中出现淡黄色浑浊,说明SO2具有 。
a.氧化性 b.还原性 c.漂白性
(3)若试剂X为Ca(ClO)2溶液,可观察到白色沉淀生成,完成该过程的离子方程式:
 。
。
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中化学试卷(解析版) 题型:填空题
如图是广州亚运会开幕式“红棉花开迎宾来”焰火盛宴的一个场景,

请回答下列问题:
(1)焰火利用了部分金属的元素特征的 反应,该反应属于 (填“物理”或“化学”)变化。
(2)现在有一种火焰的引发是当浓H2SO4滴下去跟氯酸钾起作用时,便生成了奇臭的二氧化氯气体,且发现只有氯元素的化合价发生变化。请写出该反应的方程式 。
(3)如图所示的五元环代表A、B、C、D、E五种化合物,
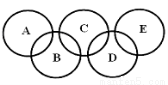
圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素组成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为 ,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2。根据以上信息回答下列问题:
,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2。根据以上信息回答下列问题:
①D的化学式是_________.
②A、B、E中均含有的一种元素名称为______________。
③B的电子式是______________。
④C与纯碱反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中化学试卷(解析版) 题型:选择题
某合作学习小组讨论辨析以下说法 ,其中说法正确的是
①纯碱和熟石灰都是碱;
②沼气和水蒸气都是可再生能源;
③冰和干冰既是纯净物又是化合物;
④硫酸和食醋既是化合物又是酸;
⑤不锈钢和目前流通的硬币都是合金;
⑥粗盐和酸雨都是混合物。
A.③⑤⑥ B.②④⑥ C.①③⑤ D.①②③⑥
查看答案和解析>>
科目:高中化学 来源:2015届福建省高二上学期半期联考化学试卷(解析版) 题型:选择题
用惰性电极实现电解,下列说法正确的是
A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变
B.电解稀氢氧化钠溶液,要消耗OH-,故需加NaOH固体才能恢复到原溶液
C.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1∶1
D.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1∶2
查看答案和解析>>
科目:高中化学 来源:2015届福建省高二上学期半期联考化学试卷(解析版) 题型:选择题
①4Al(s)+3O2(g)===2Al2O3(s) ΔH=-2834.9 kJ·mol-1
②4Al(s)+2O3(g)===2Al2O3(s) ΔH=-3119.1 kJ·mol-1
由此得出的正确结论是
A.等质量的O2比O3能量高,由O2变为O3为放热反应
B.等质量的O2比O3能量低,由O2变为O3为吸热反应
C.O3比O2稳定,由O2变为O3为吸热反应
D.O2比O3稳定,由O2变为O3为放热反应
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期半期联考化学试卷(解析版) 题型:选择题
下列化学用语书写正确的是
A.熔融状态下NaHSO4电离方程式:NaHSO4=Na++H++SO42-
B.碳酸氢铵溶液中加入足量氢氧化钠:HCO + OH-=CO32-+ H2O
C.钠投入水中:2Na+2H2O=2Na++2OH-+H2↑
D.氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三9月月考化学试卷(解析版) 题型:填空题
(12分)X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍。A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示。
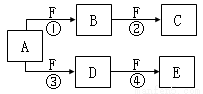
回答下列问题:
(1)A的电子式为______________。
(2)A和E反应生成G,C与G中都含有_______________(填化学键的类型)。 (3)反应③中如果转移的电子为3 mol,则被氧化的A为__________mol。
(4)科学家发明了使ZX3直接用于燃料电池的方法,其装置用铂作电极,加入碱性电解质溶液,往一极通入空气,另一电极通入ZX3并使之转化为无污染的气体,试写出负极的电极反应式:_____________________________________________________。
(5)由Z、X两元素形成的含10个电子的阳离子可和XSO4-形成一种盐A,若往A的溶液中缓缓滴入稀NaOH溶液至溶液恰好呈中性,则溶液中所含离子浓度由大到小的顺序为:___________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com