
| A�� | ��������NaHCO3��Na2CO3���������ᷴӦ������ͬ������Na2CO3������CO2���С | |
| B�� | �����ʵ�������������ͬŨ��������ȫ��Ӧ����������������Na2CO3��NaHCO3������ | |
| C�� | ������NaHCO3��Na2CO3��������ȫ��Ӧ��ǰ����������϶� | |
| D�� | �����ʵ�����NaHCO3��Na2CO3���������ᷴӦ����CO2һ���� |
���� ��������NaHCO3��Na2CO3��Na2CO3�����ʵ�����С�������ʵ���ʱ�����ɶ�����̼��ͬ����Ϸ�Ӧ�Ļ�ѧ����ʽ�����⣮
��� �⣺A�����ݷ�Ӧ�ķ���ʽNa2CO3+2HCl=2NaCl+CO2��+H2O��NaHCO3+HCl=NaCl+CO2��+H2O��֪��106g̼������ȫ��Ӧ����1mol������̼��84g̼��������ȫ��Ӧ����1mol������̼����A��ȷ��
B���ɷ���ʽNa2CO3+2HCl=2NaCl+CO2��+H2O��NaHCO3+HCl=NaCl+CO2��+H2O��֪�������ʵ�������������ͬŨ��������ȫ��Ӧ����������������Na2CO3��NaHCO3����������B��ȷ��
C����������NaHCO3��Na2CO3��������ȫ��Ӧ��Na2CO3��������϶࣬��C����
D���ɷ���ʽNa2CO3+2HCl=2NaCl+CO2��+H2O��NaHCO3+HCl=NaCl+CO2��+H2O��֪�������ʵ�������������ͬŨ��������ȫ��Ӧ�����ɶ�����̼һ���࣬��D��ȷ��
��ѡC��
���� ���⿼����̼���ƺ�̼�����Ƶ����ʣ�Ϊ��Ƶ���㣬��Ŀ�ѶȲ�����ȷ���ʵ����ʡ������йػ�ѧ����ʽ�ļ����ǽ���ؼ���ע��̼���������ᷴӦ��ԭ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Q2��Q1��57.3 | B�� | Q1=57.3��Q2 | C�� | Q2��57.3��Q1 | D�� | Q2=57.3��Q1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
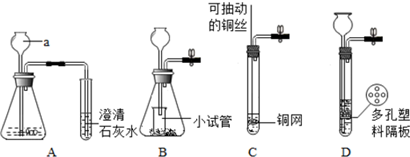
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
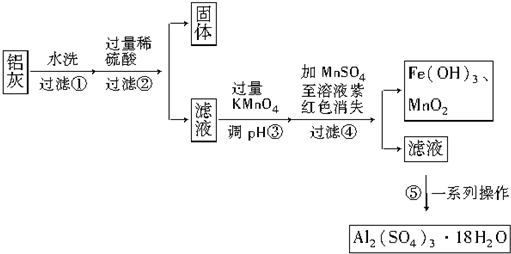
| Al��OH��3 | Fe��OH��2 | Fe��OH��3 | |
| ��ʼ����ʱ | 3.4 | 6.3 | 1.5 |
| ��ȫ����ʱ | 4.7 | 8.3 | 2.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ӽ������������Ӽ���ڵľ������� | |
| B�� | ֻ�н����ͷǽ�������ʱ�����γ����Ӽ� | |
| C�� | �������Ӽ��Ļ�����һ�������ӻ����� | |
| D�� | �ڢ�A��͵ڢ�A��Ԫ��ԭ�ӻ���ʱ��һ���γ����ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ������ϩ������ϩ����ʹ���Ը��������Һ��ɫ | |
| B�� | ����ʽΪC4H7ClO2������NaHCO3����CO2���л�����ܽṹ��3�� | |
| C�� | 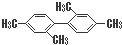 ������������11��̼ԭ�Ӵ���ͬһƽ���� ������������11��̼ԭ�Ӵ���ͬһƽ���� | |
| D�� | 1mol�л��� 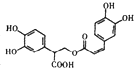 һ���������ܺ�7molNaOH��Ӧ һ���������ܺ�7molNaOH��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
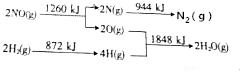
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H+��Cu2+��Cl-��SO42- | B�� | HCO3-��NO3-��SO42-��Na+ | ||
| C�� | Cl-��SO42-��K+��Na+ | D�� | Fe3+��SO42-��Cl-��Al[��OH��4]- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com