
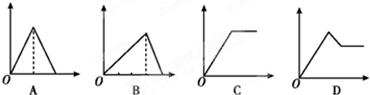


科目:高中化学 来源: 题型:
| A、在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 |
| B、乙醇、乙酸和甲醛广泛应用于食品加工 |
| C、计算机芯片所用的材料是高纯度的二氧化硅 |
| D、捕获工业排放的CO2能降低地球的温室效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||||||||||
| B、11.7g食盐晶体中的分子数为0.2×6.02×10-23 | ||||||||||
| C、等量的白磷蒸气和白磷固体分别完全燃烧,后者放出热量多 | ||||||||||
| D、根据分散系的稳定性大小将混合物分为胶体、溶液和浊液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
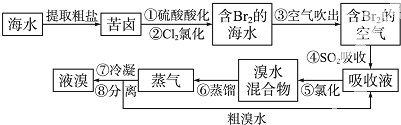
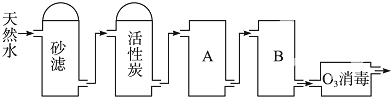
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
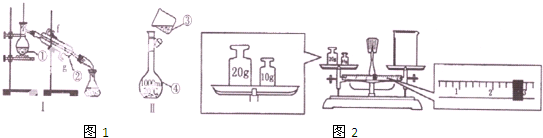
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)材料是人类赖以生存和发展的重要物质基础.
(1)材料是人类赖以生存和发展的重要物质基础.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com