
| A. | 2g D216O中含有的质子数、中子数和电子数均为NA | |
| B. | 标准状况下,22.4L SO3含有的共价键数目为3NA | |
| C. | 80g CuO和Cu2S的混合物中,所含铜原子数为NA | |
| D. | 常温常压下,16g O2作氧化剂时转移电子数不一定为2NA |
分析 A、求出重水的物质的量,然后根据重水中含质子、中子和电子数均为10个来分析;
B、标况下三氧化硫为固体;
C、Cu2S的摩尔质量是CuO的2倍,含有的铜原子也是CuO的2倍,故混合物可以看做是由“CuO“构成的;
D、氧气反应后可能变为-2价,也可能变为-1价.
解答 解:A、2g重水的物质的量为0.1mol,而重水中含质子、中子和电子数均为10个,故0.1mol重水中含中子数、电子数和质子数均为NA个,故A正确;
B、标况下三氧化硫为固体,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、Cu2S的摩尔质量是CuO的2倍,含有的铜原子也是CuO的2倍,故混合物可以看做是由“CuO“构成的,而80g混合物中含有的”CuO“的物质的量为1mol,故含铜原子为NA个,故C正确;
D、氧气反应后可能变为-2价,也可能变为-1价,故16g氧气即0.5mol氧气反应后转移的电子数可能为2NA个,还可能为NA个,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:实验题
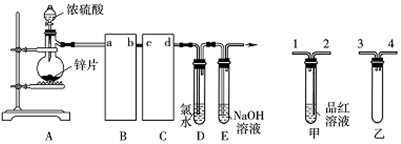
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
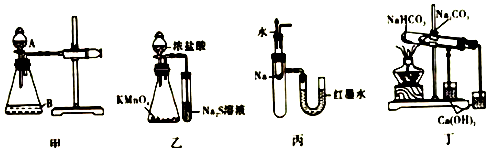
| A. | 图甲中,为检查装置的气密性,可关闭分液漏斗A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否复原 | |
| B. | 图已中,可以比较KMnO4、Cl2和S氧化性的相对强弱 | |
| C. | 将胶头滴管中的水滴入到金属钠中,能看到U型管右侧红墨水上升 | |
| D. | 图丁中,可用装置验证NaHCO3和Na2CO3的热稳定性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
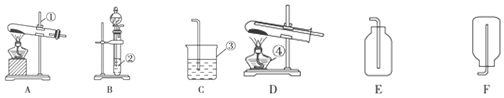
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
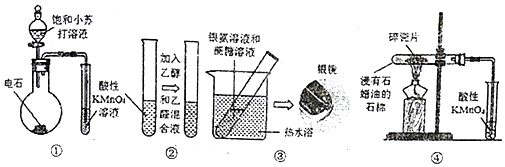
| A. | 装置①:制取乙炔并验证炔烃的性质 | |
| B. | 装置②:检验乙醇的还原性,溶液颜色从紫红色色变无色 | |
| C. | 装置③:产生银镜,说明蔗糖分子中含有醛基官能团 | |
| D. | 装置④:酸性KMnO4溶液中出现气泡且逐渐褪色,说明有不同于烷烃的另一类烃产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池输出电能的能力,取决于组成原电池的反应物的氧化还原能力 | |
| B. | 电解质溶液的导电过程,就是电解质溶液的电解过程 | |
| C. | 铅蓄电池放电时的负极和充电时的阳极均发生还原反应 | |
| D. | 电化学腐蚀和化学腐蚀都是金属原子失去电子而被氧化的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
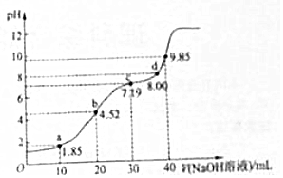 25℃时,向20mL 0.1mol•L-1H2R(二元弱酸)溶液中滴加0.1mol•L-1NaOH溶液,溶液pH与加入NaOH溶液体积的关系如图所示,下列有关说法正确的是( )
25℃时,向20mL 0.1mol•L-1H2R(二元弱酸)溶液中滴加0.1mol•L-1NaOH溶液,溶液pH与加入NaOH溶液体积的关系如图所示,下列有关说法正确的是( )| A. | a点所示溶液中:c(H2R)+c(HR-)+c(R2-)=0.1mol•L-1 | |
| B. | b点所示溶液中:c(Na+)>c(HR-)>c(H2R)>c(R2-) | |
| C. | 对应溶液的导电性:b>c | |
| D. | a,b,c,d中,d点所示溶液中水的电离程度最大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I | B. | F | C. | H | D. | Mn |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | X溶液 | 固体Y | Z溶液 | 现象 | 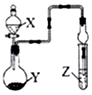 |
| A | 浓硝酸 | Cu | 淀粉KI溶液 | 溶液变为蓝色 | |
| B | 浓氨水 | 碱石灰 | AlCl3溶液 | 先产生白色沉淀后溶解 | |
| C | 稀硫酸 | Na2O2 | H2S溶液 | 产生淡黄色沉淀 | |
| D | 稀盐酸 | CaCO3 | Na2SiO3溶液 | 产生白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com