
【题目】下列物质的性质比较,正确的是
A. 酸性:H2SO4>HClO4 B. 碱性:NaOH>KOH
C. 非金属性:Si>P D. 气态氢化物稳定性: H2O>H2S
科目:高中化学 来源: 题型:
【题目】3.2g铜与过量硝酸(8 mol·L-1,30 mL)充分反应,硝酸的还原产物为NO2和NO,反应后溶液中含a mol H+,则此时溶液中所含NO3-的物质的量为( )
A.(0.2+a)mol B.(0.1+a)mol
C.(0.05+a)mol D.a mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生物体内含量极少,但必不可少的化学元素有( )
A. Fe Mn Zn Mg
B. Zn Cu Mn Ca
C. H 0 Na Mg
D. Zn Cu B Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程或现象与盐类水解无关的是( )
A. 纯碱溶液滴入酚酞变红
B. 铁在潮湿的环境下生锈
C. 加热氯化铁溶液颜色变深
D. 用氯化铵溶液除去铁锈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别取40mL的0.50mol/L盐酸与40mL0.55mol/L氢氧化钠溶液进行中和热的测定.下列说法错误的是( )

A.稍过量的氢氧化钠是确保盐酸完全反应
B.仪器A的名称是环形玻璃搅拌棒
C.在实验过程中,把温度计上的酸用水冲洗干净后再测量NaOH溶液的温度
D.用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液,结果也是正确的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷与氧气可发生如下反应:P4+5O2 == P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P akJ·mol-1、P—O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。根据图示的分子结构和有关数据估算该反应的ΔH,其中正确的是( )

A.(6a+5d-4c-12b)kJ·mol-1 B.(4c+12b-6a-5d)kJ·mol-1
C.(4c+12b-4a-5d)kJ·mol-1 D.(4a+5d-4c-12b)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系![]() ,下列有关物质的推断不正确的是
,下列有关物质的推断不正确的是
A.若甲为焦炭,则丁可能是O2 B.若甲为Fe,则丁可能是盐酸
C.若甲为SO2,则丁可能是氨水 D.若甲为NaOH 溶液,则丁可能是H2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程,属于放热反应的是( )
①工业合成氨 ②酸碱中和反应 ③水蒸气变成液态水 ④固体NaOH溶于水 ⑤Na在Cl2中燃烧 ⑥食物腐败 ⑦浓H2SO4稀释
A. ①②③④⑤⑥⑦ B. ②③④⑤ C. ①②⑤⑥ D. ①②⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据下列甲、乙、丙三图,判断下列叙述不正确的是( )
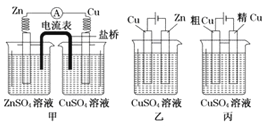
A.甲是原电池,乙是电镀装置 B.甲、乙装置中,锌极上均发生氧化反应
C.乙、丙装置中,阳极均发生氧化反应而溶解 D.丙装置中,铜电极的质量有增有减
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com