
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成的。由蛇纹石制取碱式碳酸镁的实验步骤如下:
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是________。
(2)进行Ⅰ操作时,控制溶液的pH=7~8(有关氢氧化物沉淀的pH见下表),Ca(OH)2不能过量,若Ca(OH)2过量可能会导致____________溶解,___________沉淀。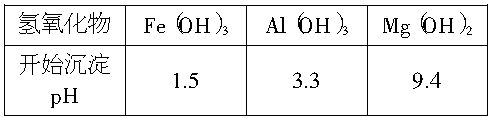
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入_________ (填物质的化学式),然后_____________________ (依次填写实验操作名称)。
(4)物质循环使用能节约资源。上述实验中,可以循环使用的物质是____________ (填写物质的化学式)。
(5)为确定产品aMgCO3?bMg(OH)2?cH2O中a、b、c的值,请完成下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量;②高温分解;③_______;④________;⑤MgO称量。
(6)18.2g产品完全分解后产生6.6gCO2和8.0g MgO,由此可知,产品的化学式中a=______、b=_______、c=______。
(1)Fe3+、Al3+
(2)Al(OH)3;Mg(OH)2
(3)NaOH ;过滤、洗涤、灼烧
(4)CO2
(5)测定CO2的质量;测定水蒸气的质量
(6)3; 1;3
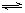 Fe(OH)3+3H+和Al3++3H2O
Fe(OH)3+3H+和Al3++3H2O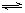 Al(OH)3+3H+,只要加入一种能消耗H+的物质即可使上述水解平衡向正反应方向移动,除去Fe3+、Al3+,该方案使用加Ca(OH)2的方法,但此步加入Ca(OH)2不能太多,需将溶液的pH控制在7~8,若pH小于7,Al3+不能完全沉淀;若pH过高导致生成的Al(OH)3又发生反应Al(OH)3+OH-=
Al(OH)3+3H+,只要加入一种能消耗H+的物质即可使上述水解平衡向正反应方向移动,除去Fe3+、Al3+,该方案使用加Ca(OH)2的方法,但此步加入Ca(OH)2不能太多,需将溶液的pH控制在7~8,若pH小于7,Al3+不能完全沉淀;若pH过高导致生成的Al(OH)3又发生反应Al(OH)3+OH-=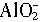 +2H2O而溶解,同时Mg2+也转化为沉淀而损失。
+2H2O而溶解,同时Mg2+也转化为沉淀而损失。 (a+b)MgO+aCO2↑+(b+c)H2O↑,需要测定的数据是①样品质量;②MgO质量;③生成CO2的质量(或体积);④生成水的质量。
(a+b)MgO+aCO2↑+(b+c)H2O↑,需要测定的数据是①样品质量;②MgO质量;③生成CO2的质量(或体积);④生成水的质量。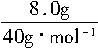 =0.2mol,n(CO2)=
=0.2mol,n(CO2)=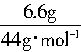 =0.15mol ,n(H2O)=
=0.15mol ,n(H2O)=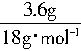 =0.2mol,得:a∶b∶c=0.15∶0.05∶0.15=3∶1∶3,所以a=3、b=1、c=3。
=0.2mol,得:a∶b∶c=0.15∶0.05∶0.15=3∶1∶3,所以a=3、b=1、c=3。 

科目:高中化学 来源: 题型:

| 金属阳离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀的pH |
| Fe3+ | 1.9 | 3.2 |
| Mg2+ | 9.4 | 11.6 |
| ||
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:

| 金属阳离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Mg2+ | 9.4 | 11.6 |
| ||
| 熔融 |
| ||
| 熔融 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 金属阳离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Mg2+ | 9.4 | 11.6 |

| ||
| 熔融 |
| ||
| 熔融 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
查看答案和解析>>
科目:高中化学 来源:2012年苏教版高中化学选修2 2.4 镁和铝的冶炼练习卷(解析版) 题型:填空题
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如下:
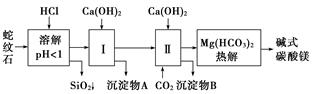
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是__________________。
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见下表)。
|
氢氧化物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
|
开始沉淀pH |
1.5 |
3.3 |
9.4 |
Ca(OH)2不能过量,若Ca(OH)2过量可能会导致________溶解、________沉淀。
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入_____________________ ___________________________________________________(填入物质的化学式),
然后______________________________________________________________________(依次填写实验操作名称)。
(4)物质循环使用,能节约资源。上述实验中,可以循环使用的物质是________(填写物质化学式)。
(5)现设计一个实验,确定产品aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量
②高温分解
③________________________________________________________________________
④________________________________________________________________________
⑤MgO称量
(6)18.2 g产品完全分解后,产生6.6 g CO2和8.0 g MgO,由此可知,产品的化学式中:
a=________,b=________,c=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com