AB
分析:A、碳酸根离子是多元弱酸阴离子分步水解;
B、电解池中铜做阳极铜失电子发生氧化反应;
C、醛基被银氨溶液氧化为醋酸,结合氨气生成醋酸铵;
D、重铬酸根离子具有强氧化性能氧化乙醇为乙酸,本身颜色变化.
解答:A、用Na
2CO
3溶液作洗涤剂,因为碳酸根离子水解显碱性:CO
32-+H
2O?HCO
3-+OH
-;HCO
3-+H
2O?H
2CO
3+2OH
-,故A错误;
B、用铜作电极电解氢氧化钠溶液,铜做阳极是活性电极,铜失电子发生氧化反应:Cu+2H
2O

2H
2↑+Cu(OH)
2↓,故B错误;
C、醛基被银氨溶液氧化为醋酸,结合氨气生成醋酸铵;“银镜反应”的离子方程式为:RCHO+2Ag(NH
3)
2++2OH
- 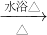
2Ag+RCOO
-+NH
4++3NH
3+H
2O,故C正确;
D、重铬酸根离子具有强氧化性能氧化乙醇为乙酸,本身颜色变化,反应的离子方程式为:2Cr
2O
72-+3C
2H
5OH+16H
+=4Cr
3++3CH
3COOH+11H
2O,故D正确;
故选AB.
点评:本题考查离子方程式的书写方法和注意问题,反应实质的理解和掌握是解题关键,题目难度中等.

 2H2↑+O2↑
2H2↑+O2↑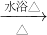 2Ag+RCOO-+NH4++3NH3+H2O
2Ag+RCOO-+NH4++3NH3+H2O 2H2↑+Cu(OH)2↓,故B错误;
2H2↑+Cu(OH)2↓,故B错误;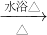 2Ag+RCOO-+NH4++3NH3+H2O,故C正确;
2Ag+RCOO-+NH4++3NH3+H2O,故C正确;
