
分析 (1)钠离子的焰色反应为黄色;
(2)使湿润的红色石蕊试液变蓝的气体是氨气;
(3)硫酸钡是一种白色不溶于酸的白色沉淀;
(4)加入少量稀硝酸使溶液酸化,再加入硝酸银溶液,产生白色沉淀,生成氯化银.
解答 解:(1)只有钠离子的焰色反应为黄色,取少量原溶液进行焰色反应,火焰呈黄色,说明原溶液中一定含有钠离子,故答案为:①;
(2)使湿润的红色石蕊试液变蓝的气体是氨气,铵根离子可以和强碱加热反应生成氨气,所以一定含有铵根离子,故答案为:③;
(3)取原溶液加入少量盐酸使溶液酸化,再加入氯化钡溶液,产生白色沉淀,说明原溶液中一定含有的离子是SO42-,故答案为:④;
(4)加入少量稀硝酸使溶液酸化,再加入硝酸银溶液,产生白色沉淀,生成氯化银,说明含有氯离子,故答案为:②.
点评 本题考查物质的检验及鉴别,为高频考点,把握常见离子之间的反应、离子检验等为推断的关键,侧重分析与推断能力的综合考查,题目难度不大.


科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
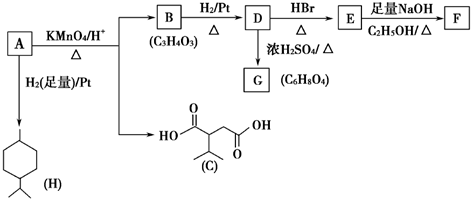
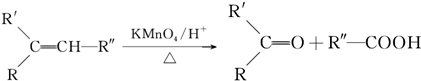
 .
.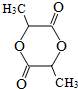 .
.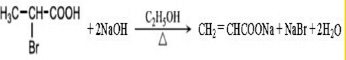 .
.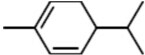 ,A与等物质的量的Br2进行加成反应的产物共有3种(不考虑立体异构).
,A与等物质的量的Br2进行加成反应的产物共有3种(不考虑立体异构).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KNO3 CH3COOH | B. | HCl NaHSO4 | C. | NaCl BaSO4 | D. | NH3•H2O H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
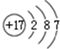 .
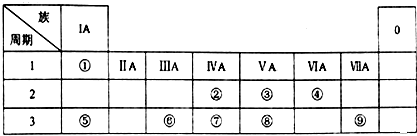
. ⑧的最高价氧化物的水化物的分子式H3PO4.
⑧的最高价氧化物的水化物的分子式H3PO4. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com