

| 反应物 |
| 反应条件 |
| 反应物 |
| 反应条件 |
 ,核磁共振氢谱只有四组峰,需要从对称性的角度结合题干限制条进行去书写;
,核磁共振氢谱只有四组峰,需要从对称性的角度结合题干限制条进行去书写; 是要把醇羟基经氧化成羧基,但考虑到酚羟基容易被氧化,所以要先保护酚羟基,故邻羟基苯甲醇先与NaOH反应,保护酚羟基不被氧化,进而用氧化剂氧化醇羟基生成-COOH,中和后可生成水杨酸,据此写出制备流程.
是要把醇羟基经氧化成羧基,但考虑到酚羟基容易被氧化,所以要先保护酚羟基,故邻羟基苯甲醇先与NaOH反应,保护酚羟基不被氧化,进而用氧化剂氧化醇羟基生成-COOH,中和后可生成水杨酸,据此写出制备流程.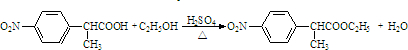 ,
,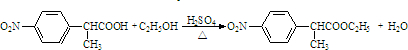
 ,a.核磁共振氢谱有四组峰,分子中含有4种等效H;b.能与FeCl3溶液发生显色反应,分子中含有酚羟基;c.能发生银镜反应,分子中含有醛基,则满足条件的结构简式为:
,a.核磁共振氢谱有四组峰,分子中含有4种等效H;b.能与FeCl3溶液发生显色反应,分子中含有酚羟基;c.能发生银镜反应,分子中含有醛基,则满足条件的结构简式为: ,
, ;
; ,
, .
.


科目:高中化学 来源: 题型:
| A、对不可回收的垃圾常用的处理方法有卫生填埋、堆肥和焚烧 |
| B、制造玻璃是复杂的物理变化,玻璃的组成不同,性能也不同 |
| C、血糖过低的患者可利用静脉注射葡萄糖溶液的方法迅速补充营养 |
| D、固体煤经处理变为气体燃料后,可以减少SO2和烟尘的污染,且燃烧效率高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
| B、正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 |
| C、正、逆反应速率都没有变化,平衡不发生移动 |
| D、正、逆反应速率都增大,平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
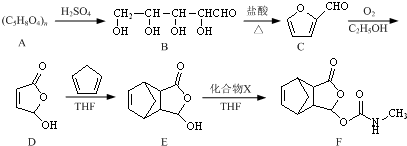
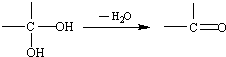
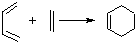
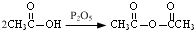
 和
和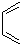 为原料合成
为原料合成 ,请设计合成路线(注明反应条件).
,请设计合成路线(注明反应条件).| 浓硫酸 |
| 170℃ |
| Br2 |
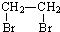
查看答案和解析>>
科目:高中化学 来源: 题型:

| 三氯甲基苯基甲醇 | 式量:224.5.无色液体.不溶于水,溶于乙醇. |
| 醋酸酐 | 无色液体.溶于水形成乙酸,溶于乙醇. |
| 结晶玫瑰 | 式量:267.5.白色至微黄色晶体.熔点:88℃.不溶于水,溶于乙醇,70℃时在乙醇中溶解度为a g. |
| 醋酸 | 无色的吸湿性液体,易溶于水、乙醇. |

| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将粗产品溶解在中,按粗产品、溶剂的质量比为1: | 得到无色溶液 | |
| ② | 将步骤1所得溶液 | ||
| ③ | 干燥步骤2所得白色晶体, | 白色晶体是结晶玫瑰 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 水解反应 | 平衡常数(K) |
| Fe3++3H2O?Fe(OH)3+3H+ | 7.9×10-4 |
| Fe2++2H2O?Fe(OH)2+2H+ | 3.2×10-10 |
| Cu2++2H2O?Cu(OH)2+2H+ | 3.2×10-7 |
| 实验内容 | 实验现象 |
| 甲同学的实验方案 | 溶液逐渐变成蓝绿色,pH略有上升 |
| 乙同学的实验方案 | 无明显现象,pH没有明显变化. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com