
 .
.分析 (1)过氧化氢在二氧化锰做催化剂的条件下生成水和氧气;
(2)氢原子和氧原子之间以共用电子对而形成水分子;
(3)1mol过氧化氢中3mol的共价键,所以H2O2有24mol共价键发生断裂,反应的过氧化氢为8mol,由2molH2O2生成4molH2O(g),则8mol的过氧化氢生成16mol的水,又因为生成1mol H2O(g)放出160.4KJ能量,所以放出热量为:160.4KJ×16=2566.4KJ;
(4)原电池是将化学能转化为电能的装置,非金属元素之间形成的化学键大多是共价键,物质的分解反应是吸热反应;氢氧燃料电池中,H2从负极通入,在反应中被氧化;根据电极反应确定pH的变化.
解答 解:(1)过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)H2O为共价化合物,各原子达到稳定结构,用电子式表示形成过程为 ,
,
故答案为: ;
;
(3)1mol过氧化氢中3mol的共价键,所以H2O2有24mol共价键发生断裂,反应的过氧化氢为8mol,由2molH2O2生成4molH2O(g),则8mol的过氧化氢生成16mol的水,又因为生成1mol H2O(g)放出160.4KJ能量,所以放出热量为:160.4KJ×16=2566.4KJ,故答案为:2566.4KJ;
(4)氢气用于燃料电池,燃料电池是将化学能转化为电能的装置,水分解时,断裂的化学键为H-O键,属于共价键,分解海水的反应属于吸热反应,氢氧燃料电池中,H2从负极通入,负极的电极反应式为:H2-2e-+2OH-=2H2O;负极上氢气和氢氧根离子反应生成水,正极上氧气得电子和水反应生成氢氧根离子,氢氧燃料电池的产物是水,KOH的物质的量不变,溶液的体积增大,浓度变小,所以PH值减小,故答案为:化学;电;共价;吸热;H2-2e-+2OH-=2H2O;不发生.
点评 本题考查化学方程式的书写、用电子式表示物质的形成、热量的转化和电极反应式的书写,综合性强,但比较容易.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
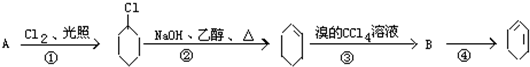
 ,名称是环己烷.
,名称是环己烷. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr+2H2O.
+2NaBr+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子排布式1s22s22p63s23p64s3违反了泡利原理 | |
| B. | 基态原子电子排布式1s22s22p63s23p63d5违反了能量最低原理 | |
| C. | 根据构造原理,原子核外电子填充顺序为1s2s2p3s3p4s3d4p5s5p4d6s4f5d6p | |
| D. | 某主族元素气态基态原子的逐级电离能分别为738、1451、7733、10540、13630、17995、21703…,当它与氯气反应时生成的阳离子是X2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 吸热反应的发生都需要加热,吸热反应都没有利用价值 | |
| B. | 若某反应正向进行时为放热反应,则该反应逆向进行时必为吸热反应 | |
| C. | 放热反应放出热量的多少与反应物的质量和状态有关 | |
| D. | 不管是吸热反应还是放热反应,升高温度,反应速率均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气是氧化剂,水是还原剂 | B. | 水被还原,氯气被氧化 | ||
| C. | 氯气既是氧化剂,又是还原剂 | D. | 该反应不是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解液的质量增加xg | B. | 阴极质量增加xg | ||
| C. | 阴极质量增加bg,b>x | D. | 阴极质量增加bg,b<x |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com