
| A、降低温度 |
| B、改用300mL1mol/L盐酸 |
| C、改用100mL3mol/L盐酸 |
| D、用等量锌粒代替锌粉 |
科目:高中化学 来源: 题型:
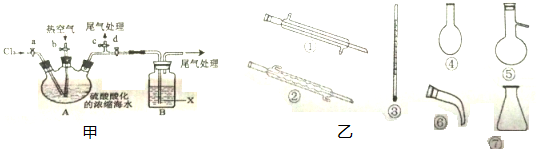
| 通入O2 |
| 通入空气吹出Br2 |
| 用X吸收 |
| 通入Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
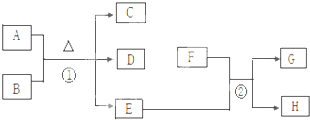 如图中A~H均为中学化学中常见的物质.已知A为紫红色金属,D能使品红溶液褪色,E为生活中常见的无色无味液体,F为黄绿色气体.请回答下列问题:
如图中A~H均为中学化学中常见的物质.已知A为紫红色金属,D能使品红溶液褪色,E为生活中常见的无色无味液体,F为黄绿色气体.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SiO2(制光纤) |
| B、氮化硅陶瓷(制导热剂) |
| C、钢化玻璃(汽车窗玻璃) |
| D、Si和Ge(半导体材料) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、①④ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCO3+2HCl=CaCl2+H2O+CO2↑ |
| B、HCl+NaOH=NaCl+H2O |
| C、Ba(OH)2+CuSO4=BaSO4↓+Cu(OH)2↓ |
| D、CuCl2+Fe=FeCl2+Cu |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com