
【题目】元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH) 4— (绿色)、Cr2O72—(橙红色)、CrO42— (黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(1)Cr3+和Al3+的化学性质相似,在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是_______,离子方程式____________________________。
(2)CrO42—和Cr2O72—在溶液中可相互转化。室温下,初始浓度为1.0mol·L1的Na2CrO4溶液中c(Cr2O![]() )随c(H+)的变化如图所示。
)随c(H+)的变化如图所示。
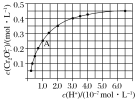
①当溶液酸性增强的时候,溶液颜色变化情况为:_________________。
②由图可知,溶液酸性增大,CrO42—的平衡转化率_________(填“增大”“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为__________。
③升高温度,溶液中CrO42—的平衡转化率减小,则该反应的ΔH_____0(填“大于”“小于”或“等于”)。(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl-,利用Ag+与CrO42—生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×105molL1)时,溶液中c(Ag+)___molL1,此时溶液中c(CrO42—)等于_____molL1 (已知Ag2CrO4、AgCl的Ksp分别为2.0×1012和2.0×1010)。
【答案】溶液蓝紫色褪去,转化为灰蓝色固体,后逐渐溶解,溶液成为绿色溶液 Cr3++3OH—===Cr(OH)3↓ Cr(OH)3+ OH—=Cr(OH)42—溶液由黄色变为橙红色增大1.0×1014(mol·L1)2小于2.0×1055.0×103
【解析】
(1)依据Cr3+与Al3+的化学性质相似,由Al3+和NaOH溶液的反应情况,不难推得,在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量的现象是:
原来Cr3+的蓝紫色的溶液,逐渐变成灰蓝色的Cr(OH)3沉淀,离子方程式为:Cr3++3OH-= Cr(OH)3![]() ,而后又逐渐溶解变为Cr(OH)4-的绿色溶液,离子方程式为:Cr(OH)3+ OH-= Cr(OH)4-;
,而后又逐渐溶解变为Cr(OH)4-的绿色溶液,离子方程式为:Cr(OH)3+ OH-= Cr(OH)4-;
(2)①从方程式及图示看出,随着酸性的增强,Cr2O72-的浓度逐渐升高,所以溶液由黄色变为橙红色;
②从方程式及图示看出:该转化随着溶液酸性增大,CrO42的平衡转化率将增大。从题给图示中,该反应的A点时c(H+)=10-7mol·L1,c(Cr2O72)=0.25 mol·L1,由Cr元素守恒,c(CrO42-)=1-2×0.25=0.5 mol·L1,故该转化的平衡常数K=0.25/(0.52×10-7×10-7)=1014;
③若温度升高,溶液中CrO42的平衡转化率减小,则该反应平衡逆向移动,该转化为放热反应,其ΔH小于0。
(3)由沉淀的溶度积计算c(Ag+)=Ksp(AgCl)/c(Cl-)=2.0×1010/1.0×105=2.0×10–5。在该溶液中c(CrO42-)= Ksp(Ag2CrO4)/c2(Ag+)=2.0×1012/(2.0×105)2=5×10-3mol·L1。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学为了制备氯气并探究其性质,回答下列问题。
Ⅰ.写出实验室制取氯气的离子方程式:_______________________________
Ⅱ.甲同学设计如图所示装置研究氯气能否与水发生反应.气体a是含有少量空气和水蒸气的氯气.请回答下列问题:

(1)浓硫酸的作用是___________________。
(2)证明氯气和水反应的实验现象为__________。
(3)ICl的性质与Cl2类似,写出ICl与水反应的化学方程式是______________________。
(4)若将氯气通入石灰乳制取漂白粉,反应的化学方程式是______________________。漂白粉溶于水后,遇到空气中的CO2,即产生漂白、杀菌作用,反应的化学方程式是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】降低大气中CO2的含量及有效地开发利用CO2,已引起了全世界的普遍重视
(1)CO2加氢合成DME(二甲醚)是解决能源危机的研究方向之一。
①2CO2(g) + 6H2(g)![]() CH3OCH3(g) + 3H2O(g) △H= -122.4kJ·mol-1
CH3OCH3(g) + 3H2O(g) △H= -122.4kJ·mol-1
某温度下,将2.0 mol CO2(g) 和6.0 mol H2(g)充入容积为2 L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中 CH3OCH3(g) 的物质分数变化情况如图所示,则P1_______P2(填“>”“<”或“=”,下同)。若T1、P1,T3、P3时平衡常数分别为K1、K3,则K1________K3,T1、P1时H2的平衡转化率为______________。

②在恒容密闭容器里按体积比为1∶3充入二氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列能说明平衡一定向逆反应方向移动的是______(填序号)。
A.反应物的浓度增大 B.混合气体的密度减小
C.正反应速率小于逆反应速率 D.氢气的转化率减小
(2)将一定量的CO2气体通入氢氧化钠的溶液中,向所得溶液中边滴加稀盐酸边振荡至过量、产生的气体与加入盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。请回答:当加入HCl 的物质的量为1 mol时,溶液中所含溶质的化学式__________,a点溶液中各离子浓度由大到小的关系式为____________________________________。

(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp = 2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若混合前Na2CO3溶液的浓度为2×10-4 mol·L-1,则生成沉淀加入CaCl2溶液的最小浓度为___________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是
A. 0.1 mol N2的质量是2.8 g
B. Mg的摩尔质量是24 g/mol
C. 2 L 0.1mol·L-1NaCl溶液中,c(Na+)=0.2mol·L-1
D. 标准状况下,11.2 L O2含有的原子数目约为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学进行有关铜、硝酸、硫酸化学性质的实验,实验过程如图所示:

①、③均观察到实验现象:溶液呈蓝色,试管口有红棕色气体产生。下列说法正确的是
A. ①试管口有红棕色气体产生,原因是硝酸被还原为NO2
B. 由③的现象可得出结论:Cu可与稀硫酸反应
C. ③中反应的离子方程式:3Cu+2NO3-+8H+ === 3Cu2++2NO↑+4H2O
D. ③中可能产生SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g)+2CO(g)![]() 2CO2(g)+S(l)△H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
2CO2(g)+S(l)△H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
A. 平衡前,随着反应的进行,容器内压强始终不变
B. 平衡时,其他条件不变,分离出硫,正反应速率加快
C. 平衡时,其他条件不变,升高温度可提高SO2的转化率
D. 其他条件不变,使用不同催化剂,该反应平衡常数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各反应中,氧化反应与还原反应在同种元素中进行的是
A.Cl2+2NaOH===NaCl+NaClO+H2O
B.2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
C.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
D.2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,水作还原剂的是
A. Mg+2H2O![]() Mg(OH)2+H2↑
Mg(OH)2+H2↑
B. 2F2+2H2O═4HF+O2
C. Cl2+H2O![]() HCl+HClO
HCl+HClO
D. 2Na2O2+2H2O═4NaOH+O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com