
【题目】下列说法不正确的是
A.离子半径(r):![]()
B.若存在简单阴离子![]() ,则X一定属于第ⅦA族元素
,则X一定属于第ⅦA族元素
C.S和Se属于第ⅥA族元素,H2S的还原性比H2Se的弱
D.元素周期表中从第ⅢB族到第ⅡB族10个纵行的元素都是金属元素
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. NaHS溶液水解的方程式为:HS﹣+H2O![]() S2﹣+H3O+
S2﹣+H3O+
B. 向H218O中投入Na2O2固体:2H218O+2Na2O2═4Na++4OH﹣+18O2↑
C. 在100 mL 2 mol/L FeBr2溶液中通入4.48 L氯气(标况下),充分反应:2Fe2++2Br﹣+2Cl2=2Fe3++Br2+4Cl-
D. 用惰性电极电解饱和氯化钠溶液:2Cl﹣+2H+![]() H2↑+Cl2↑
H2↑+Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关注饮用水,保证生活质量。请回答下列问题:
(1)饮用水中的![]() 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中![]() 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将![]() 还原为N2,其化学方程式为: 10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。
还原为N2,其化学方程式为: 10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。
上述反应中,_________元素的化合价升高,则该元素的原子_______(填“得到”或“失去”)电子。当有1mol N2生成时,反应中转移电子的数目为____________。
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上将氯气通入石灰乳 [Ca(OH)2]制取漂白粉,化学方程式为:__________________。
(3)KA1(SO4)212H2O的俗名为明矾,因其溶于水生成_____________(化学式)可以吸附杂质,从而达到净水作用。向饱和明矾溶液滴加稀氢氧化钠溶液至过量,用离子方程式和必要文字描述过程现象:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素的微粒信息如表:
元素代号 | Q | R | X | Z |
微粒信息 | 离子: | 单质分子:R2 | 离子:X3+ | 一种原子: |
已知Q、R、X都在第三周期,R2常温常压下为黄绿色气体。
完成下列填空:
(1)Q在周期表的位置是:___。化合物Q2Z的电子式为___。
(2)Q、R、X的原子半径由大到小的顺序为___(用元素符号表示);Q、R、X、Z中金属性最强的是___(用元素符号表示)。
(3)Q与X两者的最高价氧化物对应的水化物之间发生反应的方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己烯雌酚是一种激素类药物,结构如图所示,下列有关叙述中正确的是

A.该有机物易溶于水
B.可以与Na2CO3生成2molCO2
C.该分子对称性好,所以没有顺反异构
D.该有机物分子中,最多可能有18个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔为主要原料可以合成聚氯乙烯、聚丙烯腈和氯丁橡胶,如图所示是有关合成路线图.
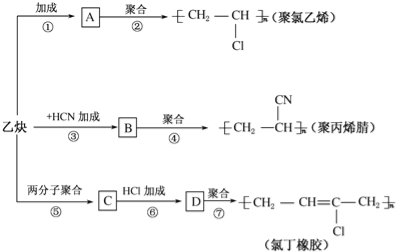
已知反应:nCH2═CH﹣CH═CH2![]()
![]()
请完成下列各题:
(1)写出物质的结构简式:A ,C .
(2)写出反应的化学方程式
反应②: ;
反应③: ;
反应⑥: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A.50mL18.4mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
B.含NA个Na+的Na2O溶解于1L水中,所得溶液中Na+的物质的量浓度为1mol·L-1
C.在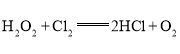 反应中,每生成32g氧气,则转移2NA个电子
反应中,每生成32g氧气,则转移2NA个电子
D.常温下,1L0.50mol·L-1NH4Cl溶液与2L0.25mol·L-1NH4Cl溶液所含![]() 物质的量相同
物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液分别滴定20.00mL浓度均为0.1mol·L-1的三种酸(HA、HB和HC)溶液,滴定的曲线如图所示,下列判断不正确的是
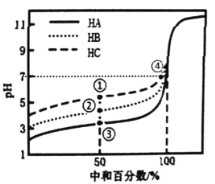
A.当中和百分数达50%时:![]()
B.滴定至①点时,溶液中:![]()
C.当中和百分数达100%时,消耗的NaOH溶液体积![]()
D.①和④所示溶液中都有:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对已经达到平衡的反应 2X(g)+Y(g)![]() 2Z(g) ΔH<0 ,下列说法正确的是( )
2Z(g) ΔH<0 ,下列说法正确的是( )
A.缩小容器体积,正、逆反应速率都增大,平衡向逆反应方向移动
B.升高反应温度,该反应的平衡常数增大
C.改变条件使平衡正向移动,反应物的转化率一定都增大
D.加入催化剂,可以降低反应所需的活化能,但不改变反应的ΔH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com