
25 ℃在25 ml、C1 mol/L的一元弱酸(HA)中,加人们v2 mL、0.1mol/L的一元强碱 (BOH)。下列有关判断十定正确的是
A.当25Cl=0.1V2时,c(A—)>c(B—) B.当pH>7时,c(A—)>c(OH—)。
C.当pH=7,且V2=25 时,C1>0.1 D.当pH<7 时,c(B+)>c(A-)
 习题精选系列答案
习题精选系列答案科目:高中化学 来源:2014-2015广东省高二上学期期中联考化学(文)试卷(解析版) 题型:?????
在我们的日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品。这里的碘、铁、钙、硒、氟应理解为
A.元素 B.单质
C.分子 D.氧化物
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市高一上学期10月月考化学试卷(解析版) 题型:填空题
(14分)已知A和B两只试管的溶液中含有K+、Ag+、Mg2+、Cl-、NO3-、OH-六种离子,向A试管中滴加酚酞溶液呈红色。请回答下列问题:
(1)A试管的溶液中含有上述离子有__________;若向A溶液中加入铝片写出该化学反应的离子方程式______________________________________________________________________;
(2)向某试管中滴加稀盐酸产生白色沉淀,则该试管为____________(填A或B);
(3)若将试管A和试管B的溶液按一定的体积比混合过滤后,蒸干可得到—种纯净物,则混合过程中发生反应的离子方程式______________、___________;
(4)若向试管A的溶液中的阳离子组成的碳酸氢盐溶液中,分别滴加盐酸和少量Ba(OH)2,则反应的离子方程式分别为_______________________、_____________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市高一上学期10月月考化学试卷(解析版) 题型:选择题
镁、铝、铜三种金属粉末混合物, 加入过量盐酸充分反应, 过滤后向滤液中加入过量烧碱溶液, 再过滤,滤液中存在的离子有
A.AlO2- B.Cu2+ C.Al3+ D.Mg2+
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市高一上学期10月月考化学试卷(解析版) 题型:选择题
下列物质中,不能与氢氧化钠溶液发生反应的是
A.Mg B.Al(OH)3 C.Al D.CO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省江南十校高三上学期期末联考理综化学试卷(解析版) 题型:选择题
室温下,下列各组粒子在指定溶液中能大量共存的是
A.Ba(NO3)2 溶液中:SO2、Na+、NH4+、CH3COO-
B.Kw/c(H+)=0.1mol/L的溶液中:K+、Ba2+、C1-、HCO—
C.FeCl2溶液中:H2O2、Mg2+、H+、Cl-
D.含苯酚的水溶液中用::Al3+、NH4+、Br-、SO42-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高三上学期期末考试化学试卷(解析版) 题型:选择题
下列仪器能用酒精灯直接加热的是
A.烧瓶 B.容量瓶 C.试管 D.烧瓶
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高三上学期期末考试化学试卷(解析版) 题型:选择题
下列物质能与水反应放出氧气的是
A.氧化钠 B.过氧化钠 C.碳酸钠 D.硫酸钠
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省宁波市高三一月化学试卷(解析版) 题型:填空题
(14分)硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁。硫酸亚铁铵在 500℃时隔绝空气加热完全分解。回答下列问题:
(1)硫酸亚铁铵隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和 。
(2)为检验分解产物的成份,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。
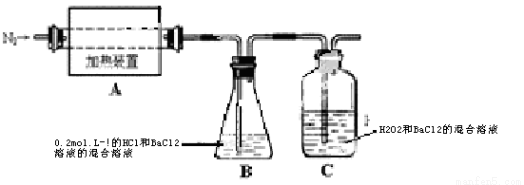
①A中固体充分加热较长时间后,通入氮气,目的是 。
②为验证A中残留物是否含有FeO,需要选用的试剂有 。
A.KSCN溶液 B.稀硫酸 C.浓盐酸 D.KMnO4溶液
③装置B中BaCl2溶液的作用是为了检验分解产物中是否有 气体生成,若含有该气体,观察到的现象为 。
④若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为bmol,C中沉淀物质的量为amol,则
b a(填“大于”、“小于”或“等于”)
⑤实验中,观察到C中有白色沉淀生成,则C中发生的反应为 (用离子方程式表示)。
(3)已知亚铁离子被氧气氧化的反应是:4Fe2+ + O2 + (4+2x) H2O 2Fe2O3?xH2O + 8H+,硫酸亚铁铵 溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。
2Fe2O3?xH2O + 8H+,硫酸亚铁铵 溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com