
分析 (1)铜是29号元素,位于周期表中第四周期,第ⅠB族,根据原子核外电子排布规律可写出Cu2+的核外电子排布式,据此答题;
(2)加热条件下,铜和浓硫酸反应生成硫酸铜、二氧化硫和水,无水硫酸铜是白色的,CuSO4•5H2O是蓝色的,显示水合铜离子特征蓝色;
(3)根据SO42-中心原子含有的共价键个数与孤电子对个数之和确定其空间构型和杂化方式;
(4)氧离子的半径小于硫离子,根据离子半径对晶格能的影响可知,半径越小,晶格能越大,物质的熔沸点就越高;
(5)N、F、H三种元素的电负性:F>N>H,所以NH3中共用电子对偏向N,而在NF3中,共用电子对偏向F,偏离N原子;
(6)元素金(Au)处于周期表中的第六周期,与Cu同族,则最外层电子数为1,以此判断电子排布式,利用均摊法计算晶胞;
(7)CaF2的结构如图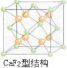 ,利用均摊法计算.
,利用均摊法计算.
解答 解:(1)铜是29号元素,位于周期表中第四周期,第ⅠB族,根据原子核外电子排布规律可写出Cu2+的核外电子排布式为1s22s22p63s23p63d9,
故答案为:ⅠB;1s22s22p63s23p63d9;
(2)加热条件下,铜和浓硫酸反应生成硫酸铜、二氧化硫和水,反应方程式为:Cu+2 H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,白色无水硫酸铜可与水结合生成蓝色的CuSO4•5H2O,显示水合铜离子特征蓝色;
故答案为:Cu+2 H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;白色无水硫酸铜可与水结合生成蓝色的CuSO4•5H2O;
(3)SO42-离子中含有4个σ键,没有孤电子对,所以其立体构型是正四面体,硫原子采取sp3杂化;
故答案为:正四面体;sp3;
(4)氧离子的半径小于硫离子,半径越小,晶格能越大,物质的熔沸点就越高,所以Cu2O的熔点比Cu2S的高;
故答案为:高;半径越小,晶格能越大,物质的熔沸点就越高;
(5)N、F、H三种元素的电负性:F>N>H,所以NH3中共用电子对偏向N,而在NF3中,共用电子对偏向F,偏离N原子,导致NF3中N原子核对其孤对电子的吸引能力增强,难以形成配位键,故NF3不易与Cu2+形成配离子;
故答案为:F的电负性大于N,NF3中,共用电子对偏向F,偏离N原子,导致NF3中N原子核对其孤对电子的吸引能力增强,难以形成配位键;
(6)元素金(Au)处于周期表中的第六周期,与Cu同族,则最外层电子数为1,则最外层电子排布式为6s1,在晶胞中Cu原子处于面心,N(Cu)=6×$\frac{1}{2}$=3,Au原子处于顶点位置,N(Au)=8×$\frac{1}{8}$=1,则该合金中Cu原子与Au原子数量之比为3:1,为金属晶体,原子间的作用力为金属键;
故答案为:6s1;3:1;金属键;
(7)CaF2的结构如图 ,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中,则H原子应位于晶胞内部,则应含有8个H,则化学式为Cu3AuH8;
,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中,则H原子应位于晶胞内部,则应含有8个H,则化学式为Cu3AuH8;
故答案为:Cu3AuH8.
点评 本题考查物质结构和性质,涉及晶胞计算、原子核外电子排布、原子杂化、空间构型判断、氧化还原反应等知识点,侧重考查学生分析计算能力,解题的难点在第(7)中对常见晶胞要熟记.


科目:高中化学 来源: 题型:解答题
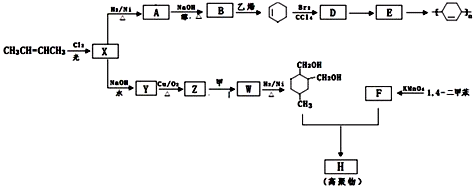
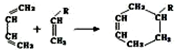 (或写成
(或写成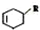 R代表取代基或氢)
R代表取代基或氢)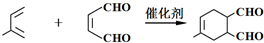 .
.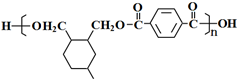 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1mol水的体积约是22.4升 | |
| B. | 1molH2所占的体积约是22.4升 | |
| C. | 标准状况下,6.02×1023个分子所占的体积约是22.4升 | |
| D. | 标准状况下,28g氮气和CO的混合气体的体积约是22.4升 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
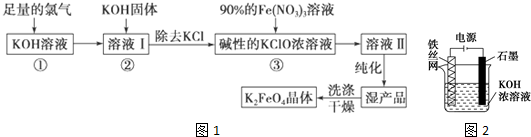
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属性:Na>Mg | B. | 热稳定性:HF>HCl | ||
| C. | 酸性:H2SO3>H2CO3 | D. | 氧化性:O2>S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
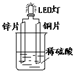
| A. | 锌片换成铁片,电路中的电流方向不变 | |
| B. | 铜电极的电极反应式为Cu2++2e-=Cu | |
| C. | 将硫酸换成柠檬汁,导线中仍有电子流动 | |
| D. | 装置中存在“化学能→电能→光能”的转换 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com