

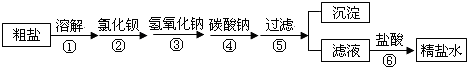
���� ����ת��ͼ��֪����Ϊ��ˮ��������Ҫ�����У������������������ӽ������ȣ�ĸҺΪ���ε��ᴿ������ɹ�����տ�����ˮ�Ͷ�����̼���������к��е⻯�ص����ʣ�����ˮ�����ݹ��˵õ����е����ӵ���Һ��ͨ�������������û����⣬�õ����ˮ��Һ�����л��ܼ���ȡ�õ�������л���Һ��������ɵõ��⣮
��1����ˮ��������Ҫ�����У������������������ӽ������ȣ�������Ϊ��ȡ��������ȡ����ѡ��ʹ�õ���Ҫ����������
��2���Լ�X��������������������Ϊ���ʵ⣻�Լ�YΪ�л���ȡ������ȡ�ⵥ�ʣ���ⲻ��Ӧ������Y�е��ܽ�ȴ�����ˮ�е��ܽ�ȺͲ�����ˮ�����߷ֲ㣩��
��3�����ݳ�ȥ����������ñ����ӳ�������ȥþ���������������ӽ��г�������ȥ��������̼������ӽ��г����������ı�������Ҫ��̼������ӳ�ȥ���з�����������Һ�м�������������õ�����ˮ���з�����
��4������Ʒ������Ʒ�ڿ����в��ױ���ʴ����Al���������������ܵ���������ֹ��Ӧ�Ľ��У����Բ��ױ���ʴ���Դ������
��� �⣺��1����ˮ��������Ҫ�����У������������������ӽ������ȣ�������Ϊ��ȡ����ȡ����ʹ�õ���Ҫ��������Ϊ��Һ©����
�ʴ�Ϊ���������ߵ������������ӽ������ȣ�����Һ©����
��2����I-��Һ�е�Ԫ�صĻ��ϼ�Ϊ-1�ۣ������е�Ԫ�صĻ��ϼ�Ϊ0�����ڷ�Ӧ�е�Ԫ�صĻ��ϼ����ߣ���Ԫ�ر����������Ժ�I-��Һ�м����Լ�X��Ŀ���ǽ�I-��������ȡ��ѡȡ����Ϊ����ȡ�������ʲ�������Ӧ����ȡ����ԭ�ܼ����������ܶȲ�ͬ����������ȡ���е��ܽ�ȴ�����ԭ�ܼ��е��ܽ�ȣ����Ե���Y�е��ܽ�ȴ�����ˮ�е��ܽ�ȺͲ�����ˮ�����߷ֲ㣩��
�ʴ�Ϊ��������������ˮ�����߷ֲ㣩��
��3��A��һ���¶��£��Ȼ��Ƶ��ܽ���ǹ̶�����ģ����������ı����ܽ�ȣ�ֻ��ӿ��Ȼ��Ƶ��ܽ��ٶȣ���A����
B���ۢܿ��Եߵ�����Ӱ�챵���ӡ�þ���ӳ�������ע���Ȼ�����̼���Ƶ�˳���ܵߵ�����B��ȷ��
C������������Ȼ�����Һ�����Խ����������ת��Ϊ�������ӹ���̼������Һ�����Խ������Ӻͷ�Ӧʣ��ı�����ת��Ϊ�������ӹ�������������Һ�����Խ�þ����ת��Ϊ���������Ԣݲ����еõ��ij����������֣���C����
D�������У��������������Ŀ���dz�ȥ�������������ƺ�̼���ƴӶ��õ��Ȼ�����Һ�����ԣ���D��ȷ��
�ʴ�Ϊ��BD��
��4����������������е�������ˮ�����ʹ�ͬ���õĽ������������е�������Ӧ���������ܵ�������Ĥ���������ã��������ʻ��õ����ڿ����в�����ʴ��
�ʴ�Ϊ�����ڿ��������γ�һ�����ܵ�����Ĥ��
���� �����ص㿼���˻�ѧ����Դ�ۺ����á����������ȷ����֪ʶ���������ý�������ͺ�ˮ��Դ���¿γ̱��̲��еı������ݣ��ڸ߿�������Ҳ�������֣����������е�����ʯ��������������ݣ���ˮ��Դ��صĺ�ˮ���塢��ˮ��þ���Ǹ߿�������ȵ㣬ֻ�����պ���ص���������ѧ�����Լ�����ʵ�鼼�ܾ���˳�������Ŀ�Ѷ��еȣ�


 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
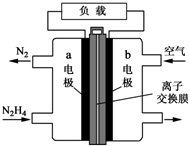 ��Ԫ�ص��⻯����������ڹ�ҵ�������������ж��й㷺Ӧ�ã��ش��������⣺
��Ԫ�ص��⻯����������ڹ�ҵ�������������ж��й㷺Ӧ�ã��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
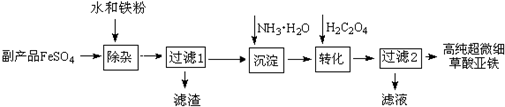
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Թ���Һ����ɫ�������Թ���Һһ����Ѫ��ɫ | |
| B�� | ���Թ���Һ����ɫ�����Թ����Ϻ�ɫ��ȥ��˵���μ���ˮ�����Һ��һ���� Fe3++ | |
| C�� | ���Թ���Һ��Ѫ��ɫ������Թ���Һ�����ܳ���ɫ | |
| D�� | �����Թ���Һ��Ѫ��ɫ����Ҳ������ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
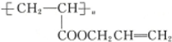 ����A�Ľṹ��ʽΪ ��������
����A�Ľṹ��ʽΪ ��������| A�� | CH3CH2CH2OH | B�� | CH2�TCHCH2OH | C�� | 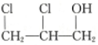 | D�� | 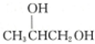 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��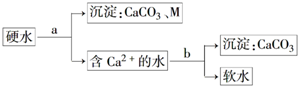
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com