
分析 (1)氮原子的摩尔质量是14g/mol;氧原子的物质的量为硝酸的3倍;
(2)MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O反应中浓盐酸的作用为酸性和还原性;制得氯气11.2L(标准状况),即0.5mol时,转移电子为1mol,则转移电子数为6.02×1023;
故答案为:6.02×1023.
解答 解:(1)氮原子的摩尔质量是14g/mol;氧原子的物质的量为硝酸的3倍,所以1mol HNO3约含有3NA,故答案为:14g/mol;3NA;
(2)MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O反应中浓盐酸的作用为酸性和还原性;制得氯气11.2L(标准状况),即0.5mol时,转移电子为1mol,则转移电子数为6.02×1023;
故答案为:酸性和还原性;6.02×1023.
点评 本题考查了物质的量的相关计算和氧化还原反应,侧重于氧化还原反应概念及电子转移的考查,题目难度不大,注意从化合价的角度分析.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 钠在空气中燃烧,生成淡黄色的氧化钠粉末 | |
| B. | 钠是一种强还原剂,可以把钛从其盐溶液中置换出 | |
| C. | 将灼热的铜丝放入盛有氯气的集气瓶中,生成棕黄色的雾 | |
| D. | Fe(OH)3胶体具有吸附性,能吸附水中的悬浮颗粒并沉降,因而可用于净水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | 用大理石盐酸反应制取CO2 气体,立即通入一定浓度Na2SiO3 溶液中 | 出现白色沉淀 | H2CO3酸性比H2SiO3酸性强 |
| B | 向某溶液先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中含有SO42-、SO32-、HSO3-中一种几种 |
| C | 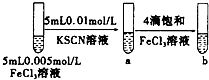 | 试管b比试管a中溶液红色深 | 增大反应物浓度,平衡向正反应方向移动 |
| D | 等体积PH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | HA放出的氢气多且反应速率快 | HA酸性比HB强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H12O6(葡萄糖aq)+6O2$\stackrel{酶}{→}$6CO2+6H2O | |
| B. | CH3COOH+KOH?CH3COOK+H2O | |
| C. | A+B?C+D;△H<0 | |
| D. | 反应物所具有的总能量小于生成物所具有的总能量的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2溶液与少量Ca(OH)2溶液反应:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| B. | 向NaClO溶液中通入少量SO2:2ClO-+SO2+H2O═2HClO+SO32- | |
| C. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 用过量氨水吸收工业尾气中的SO2:2NH3•H2O+SO2═2NH4++SO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表中金属元素与非金属元素交界线附近的元素既具有一定的金属性也具有一定的非金属性,所以它们属于过渡元素 | |
| B. | 若M2+和N2-的核外电子层结构相同,则原子序数:N>M | |
| C. | 元素周期表的短周期元素中,最外层电子数是其电子层数2倍的元素共有4种 | |
| D. | 在元素周期表中,原子序数差值为2的两种元素有可能处于同一主族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
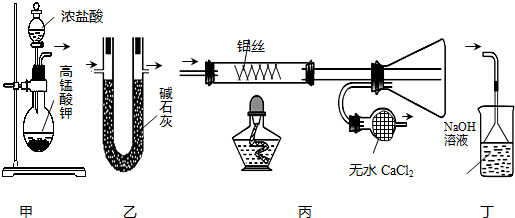
| A. | 用装置甲制取氯气 | B. | 用装置乙干燥氯气 | ||
| C. | 用装置丙制取并收集AlCl3 | D. | 用装置丁处理丙中排出的尾气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com