
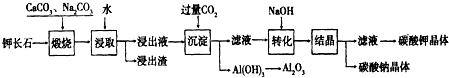
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯水具有杀菌消毒作用,其中起作用的物质是氯气 |
| B、加碘食盐中所加的“碘”一般是碘化钾 |
| C、区别氯化铁溶液和氢氧化铁胶体可以用丁达尔效应 |
| D、用干燥的有色布条可以检验氯化氢气体中是否混有氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①>②>③ |
| B、②>①>③ |
| C、③>①>② |
| D、②>③>① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.43 | 1.10 | 0.99 | 1.86 | 0.75 |
| 最高或最低化合价 | +2 | +3 | +5 | +7 | +1 | +5 | |
| -2 | -3 | -1 | -3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
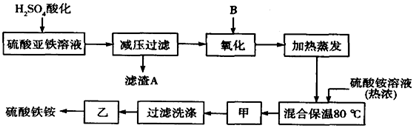
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在同温同压下,相同体积的任何气体含有相同数目的原子 |
| B、氧化还原反应的判断依据是元素化合价是否有变化 |
| C、能导电的物质一定是电解质 |
| D、金属氧化物不一定是碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com