
【题目】垃圾的再生利用是垃圾资源化的最佳途径.某垃圾箱上贴有如右图所示标志,应向此垃圾箱中丢弃的垃圾是( ) 
A.废旧电池
B.厨余垃圾
C.危险废物
D.可回收物
【答案】D
【解析】解:A.废旧电池中的镉元素,则被定为致癌物质;汞中毒,会患中枢神经疾病;电池腐烂后,其中的汞、铅、镉等重金属溶出会污染地下水和土壤,破坏人类的生存环境,废旧电池属于有害垃圾,标志为  ,故A错误;
,故A错误;
B.厨余垃圾是食品类废物,标志为  ,故B错误;
,故B错误;
C.危险垃圾的标志是  ,故C错误;
,故C错误;
D.图示与可回收垃圾的标志相同,故D正确;
故选D.
生活垃圾一般可分为四大类:可回收垃圾、厨余垃圾、有害垃圾和其它垃圾;根据不同垃圾所对应的标志确定垃圾的种类.
A.废旧电池属于有害垃圾;B.厨余垃圾是食品类废物;C.危险废物,这些垃圾需要特殊安全处理,属于有害垃圾;D.可回收垃圾主要包括废纸、塑料、玻璃、金属和布料五大类;图所示的标志为可回收物.


科目:高中化学 来源: 题型:
【题目】[化学—选修3:物质结构与性质]某硅酸盐研究所在硅酸盐材料和闪烁晶体等领域研究上取得了重大的成就。
(1)SiO44-是构成硅酸盐的基本结构单元,通过共用氧相连可形成硅氧组群。
①基态硅原子价电子排布图是________。
②与SiO44-互为等电子体的微粒符号是______(任写一种)。
③下图为一种硅氧组群的结构示意图,其离子符号为______,其中Si原子的杂化方式为____。
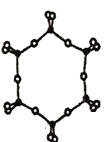
④电负性:Si______O(填“>”、“=”或“<”) 。
(2)钨酸铅(PWO)是一种闪烁晶体,晶胞结构如图所示。
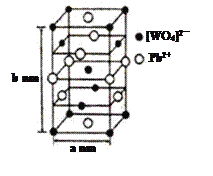
①PWO中钨酸根结构式式为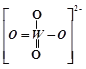 ,该离子中δ键和π键的个数比是______。
,该离子中δ键和π键的个数比是______。
②PWO晶体中含有的微粒间作用力是______(填标号)。
A.范德华力 B.离子键
C.共价键 D.金属键
③己知晶体的摩尔质量为Mg·mol-1,则该晶体的密度d=_______g·cm-3。(阿伏加德罗常数用NA表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用钒钛磁铁矿为原料冶炼铁,产生一种固体废料,主要成分如下表。

通过下列工艺流程可以实现元素Ti、Al、Si的回收利用,并得到纳米二氧化钛和分子筛。

请回答下列问题:
(1)步骤①②③中进行分离操作的名称是____,
(2)下列固体废料的成分中,不属于碱性氧化物的是____(填字母序号)。
a. TiO2 b.MgO c.SiO2 d.CaO
(3)熔融温度和钛的提取率关系如下图,适宜温度为500℃,理由是____。

(4)滤液①中溶质的成分是____。
(5)步骤②中发生反应的离子方程式是 ___。
(6)将步骤③中制取分子筛的化学方程式补充完整:______
![]()
根据成分表中数据,计算10 kg固体废料,理论上应再加入Na2 Si03物质的量的计算式是n( Na2SiO3)=____mol(摩尔质量/g/mol :SiO2 60 Al2O3 102)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯的原子序数为17,35Cl是氯的一种同位素,下列说法不正确的是( )
A.35Cl原子所含质子数为18
B.35Cl2气体的摩尔质量为70
C.3.5g的35Cl2气体的体积为2.24L
D.1/18mol的H35Cl分子所含中子数约为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为四种短周期主族元素,它们在元素周期表中的相对位置如下图所示,其中Y原子的最外层电子数是其电子层数的2倍。下列说法正确的是

A. W单质比X单质更易与氢气化合
B. W的最高价含氧酸可用于制取氢气
C. 元素X和钠形成的化合物只含有离子键
D. 简单离子半径大小关系为:Y>Z>W>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物在工业生产和生活中都有重要的应用,运用化学原理研究氮的单质及其化合物具有重要意义。
I.一氯胺(NH2Cl)在中性或酸性环境中会发生水解,生成具有强烈杀菌作用的HClO,是重要的水的消毒剂。
(1)写出NH2C1的电子式______________________。
(2)写出NH2C1与水反应的化学方程式______________________。
(3)一定条件下(T℃、1.01×105Pa),可以用Cl2(g)和NH3(g)制得NH2Cl(g),同时得到HCl(g)。已知部分化学键的键能如下表:

写出该反应的热化学方程式____________________________________。
Ⅱ.亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO与Cl2在一定条件下合成:2NO(g)+Cl2(g) ![]() 2NOCl(g) △H<0。保持恒温恒容条件,将物质的量之和为3mol的NO和Cl2以不同的氮氯比
2NOCl(g) △H<0。保持恒温恒容条件,将物质的量之和为3mol的NO和Cl2以不同的氮氯比![]() 进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
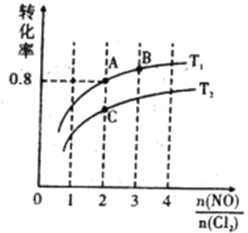
(4)图中T1、T2的关系为:T1______T2 (填“>”、“<”或“=”)
(5)图中纵坐标为物质__________的转化率,理由为___________________________。
(6)图中A、B、C三点对应的NOCl体积分数最大的是________(填“A”、“B”、或“C”)。
(7)若容器容积为1L,则B点的平衡常数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,甲、乙两烧杯盛有同浓度同体积的稀硫酸将纯锌片和纯铜片分别按图示方式插入其中,以下有关实验现象或结论的叙述正确的是
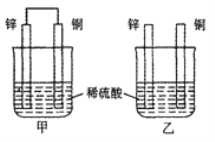
A. 两烧杯中铜片表面均有气泡产生
B. 甲中铜片是正极,乙中铜片是负极
C. 甲杯溶液的c(H+)减小,乙杯溶液的c(H+)变大
D. 产生气泡的速率甲比乙快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分。按要求填写下列空白:
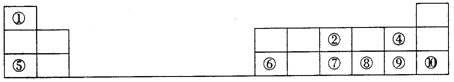
(1)元素⑦在周期表中的位置可表示为_______。
(2)①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。
(3)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是_______(用化学式表示)。
(4)⑤和⑥两种元素的最高价氧化物对应的水化物反应的离子方程式为_______。
(5)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是_______。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
(6)铁元素处在周期表第四周期第Ⅷ族,它在地壳中含量仅次于铝。全世界每年都有大量的钢铁因生锈而损失。钢铁发生电化学腐蚀时,负极反应是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁过程中发生的主要反应为 ![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g) ![]() Fe(s)+CO2(g)△H<0,欲提高上述反应CO的平衡转化率,可采取的措施是( )
Fe(s)+CO2(g)△H<0,欲提高上述反应CO的平衡转化率,可采取的措施是( )
A.提高反应温度
B.移出部分CO2
C.加入合适的催化剂
D.减小容器的容积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com