
下列叙述正确的是()
A. NaCl溶液在电流作用下电离成Na+与Cl﹣
B. 溶于水后能电离出H+的化合物都是酸
C. 液态氯化氢不能导电,但氯化氢是电解质
D. 导电性强的溶液里自由移动离子数目一定比导电性弱的溶液里自由移动离子数目多
考点: 电解质在水溶液中的电离;酸、碱、盐、氧化物的概念及其相互联系;电解质与非电解质.
专题: 电离平衡与溶液的pH专题.
分析: A.电离是在水分子作用下或者通过加热使化学键断裂离解出自由移动的离子,不需要通电;NaCl溶液在电流作用下发生的是电解;
B.酸是指电离时生成的阳离子只有氢离子的化合物;
C.在水溶液中或者熔融状态下能导电的化合物是电解质;
D.电解质导电能力强弱与自由移动的离子的浓度,所带的电荷多少有关.
解答: 解:A.NaCl溶液在电流作用下发生的是电解生成氯气、氢气、氢氧化钠,氯化钠在水溶液中或者在熔融状态下电离成Na+与Cl﹣,故A错误;
B.NaHSO4电离方程式为:NaHSO4=Na++H++SO42﹣,NaHSO4属于盐,不是酸,故B错误;
C.虽然液体氯化氢不能导电,但是氯化氢在水溶液中能导电,是化合物,属于电解质,故C正确;
D.电解质导电能力强弱与自由移动的离子的浓度,所带的电荷多少有关,故D错误;
故选:C.
点评: 本题考查了电解质、酸、电离、电解的概念,题目简单,要求同学们加强基本概念的理解和记忆,以便灵活应用,注意电离和电解的条件.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
已知下列热化学方程式:①Zn(s)+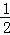 O2(g)═ZnO(s);△H1;②Hg(l)+
O2(g)═ZnO(s);△H1;②Hg(l)+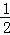 O2(g)═HgO(s);△H2.则反应Zn(s)+HgO(s)═Hg(l)+ZnO(s);△H3,△H3为( )
O2(g)═HgO(s);△H2.则反应Zn(s)+HgO(s)═Hg(l)+ZnO(s);△H3,△H3为( )
|
| A. | △H1﹣△H2 | B. | △H2﹣△H1 | C. | △H1+△H2 | D. | ﹣(△H1+△H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
稀土元素又称“二十一世纪黄金”,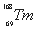 、
、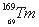 和
和 属于稀土元素,铥(Tm)可用来指导不需要电源的手提式X射线机。下列说法不正确的是
属于稀土元素,铥(Tm)可用来指导不需要电源的手提式X射线机。下列说法不正确的是
A.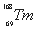 和
和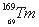 互为同位素 B.
互为同位素 B.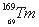 和
和 是不同的核素
是不同的核素
C.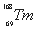 和
和 的中子数相差4 D.
的中子数相差4 D.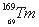 和
和 的电子数相差3
的电子数相差3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各溶液中,Na+物质的量浓度最大的是()
A. 2L 0.5mol/L NaCl溶液 B. 3L 0.3mol/L Na2SO4溶液
C. 1L 0.4mol/L Na2CO3溶液 D. 4L 0.15mol/L Na3PO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
只能表示一个化学反应的离子方程式是()
A. H++OH﹣=H2O
B. 2H++CO32﹣=H2O+CO2↑
C. Cu(OH)2+2H+=Cu2++2H2O
D. Mg2++2OH﹣+Ba2++SO42﹣=BaSO4↓+Mg(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中铁元素被还原的是()
A. 2Fe(OH)3 Fe2O3+3H2O B. Fe+CuSO4=Cu+FeSO4
Fe2O3+3H2O B. Fe+CuSO4=Cu+FeSO4
C. Fe(OH)3+3HCl=FeCl3+3H2O D. 2Fe2O3+3C 4Fe+3CO2↑
4Fe+3CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
1)请把符合要求的化学方程式的字母填在下列空白处:
①既属于分解反应又是氧化还原反应的是 .
②既属于化合反应,又是氧化还原反应的是 .
③不属于四种基本反应类型的氧化还原反应的是 .
A.(NH4)2SO3 2NH3↑+H2O+SO2↑
2NH3↑+H2O+SO2↑
B.2CO+O2 CO2
CO2
C.2C+SiO2 Si+2CO↑
Si+2CO↑
D.NH4NO3 N2O+2H2O
N2O+2H2O
E.CaCO3+CO2+H2O=Ca(HCO3)2
F.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O.
MnCl2+Cl2↑+2H2O.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是()
A. 铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑
B. 稀硫酸与氢氧化钡溶液混合:SO42﹣+Ba2+=BaSO4↓
C. 碳酸钙与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O
D. 盐酸与澄清石灰水反应:H++OH﹣═H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com