
| A. | 减小C 的浓度 | B. | 通入He气使压强增大 | ||
| C. | 减小B的浓度 | D. | 增大A或B的浓度 |
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案科目:高中化学 来源: 题型:选择题
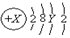 ,则X、Y及该原子3d能级上的电子数不可能的组合是( )
,则X、Y及该原子3d能级上的电子数不可能的组合是( )| A. | 18、8、0 | B. | 20、8、0 | C. | 25、13、5 | D. | 30、18、10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol•L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断正确的是( )
室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol•L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断正确的是( )| A. | 室温下,0.1 mol•L-1的三种酸溶液中由水电离产生的c(H+)的关系:HA>HB>HD | |
| B. | 滴定至P点时,溶液中c(B-)>c(Na+)>c(H+)>c(HB)>c(OH-) | |
| C. | pH=7 时,三种溶液中:c(A-)=c(B-)=c(D-) | |
| D. | 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.24L(标准状况)苯在O2中完全燃烧,得到0.6NA个CO2分子 | |
| B. | 0.1mol的11B中,含有0.6NA 个中子 | |
| C. | 标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA | |
| D. | 常温常压下,17g 羟基含有的电子总数为 7 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从左向右数第六纵行是ⅥA族 | |
| B. | 所含元素形成的化合物种类最多的族是第IVA族 | |
| C. | 七个周期18个族 | |
| D. | ⅠA族全部是金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x=4 | |
| B. | 2 min内B的反应速率为0.1 mol•(L•min)-1 | |
| C. | 混合气体密度不变,则表明该反应已达到平衡状态 | |
| D. | B的转化率为40% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0mol,1mol | B. | 0.5mol,0mol | C. | 0.25mol,.0.5mol | D. | 0.25mol,0.25mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③ | C. | ①② | D. | ①③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com