
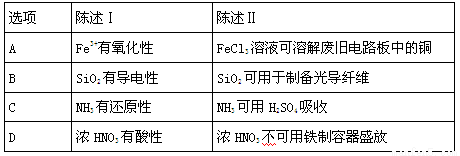
下列陈述I、II均正确且有因果关系的是
科目:高中化学 来源:2015届山东省高三10月阶段性考试化学试卷(解析版) 题型:填空题
(8分) 1 L某混合溶液中可能含有的离子如下表:
可能大量含有的阳离子 | H+ NH4+ Al3+ K+ |
可能大量含有的阴离子 | Cl- Br- I‑ ClO‑ AlO2- |
(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积(v)的关系如图所示。
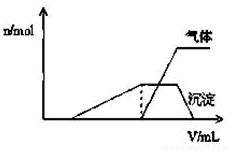
①则该溶液中确定含有的离子有 ;
②不能确定是否含有的阳离子有 ,
③要确定其存在可补充做的实验是 ;
④肯定不存在的阴离子有 。
(2)经检测,该溶液中含有大量的Cl-、Br-、I-若向1 L该混合溶液中通入一定量的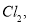 溶液中的Cl-、Br-、I-物质的量与通入Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
溶液中的Cl-、Br-、I-物质的量与通入Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
Cl2的体积(标准状况) | 2.8 L | 5.6L | 11.2L |
n(Cl-) | 1.25mol | 1.5mol | 2mol |
n(Br-) | 1.5mol | 1.4mol | 0.9mol |
n(I-) | a mol | 0 | 0 |
①当通入Cl2的体积为2.8 L时,溶液中发生反应的离子方程式为 。
②原溶液中Cl-、Br-、I-的物质的量浓度之比为 。
查看答案和解析>>
科目:高中化学 来源:2015届山东省济宁市高三10月阶段测试化学试卷(解析版) 题型:选择题
下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
A | 碳酸钠溶液可用于治疗胃病 | Na2CO3可与盐酸反应 | Ⅰ对,Ⅱ对,有 |
B | 向Na2O2的水溶液中滴入酚酞变红色 | Na2O2与水反应生成氢氧化钠 | Ⅰ对,Ⅱ错,无 |
C | 金属钠具有强还原性 | 高压钠灯发出透雾性强的黄光 | Ⅰ对,Ⅱ对,有 |
D | 过氧化钠可用于航天员的供氧剂 | Na2O2能和CO2和H2O反应生成O2 | Ⅰ对,Ⅱ对,有 |
查看答案和解析>>
科目:高中化学 来源:2015届山东省泰安市高三上学期期中考试化学试卷(解析版) 题型:填空题
(8分)已知溶液中:还原性HSO3->I-,氧化性IO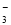 >I2>SO42-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示。
>I2>SO42-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示。
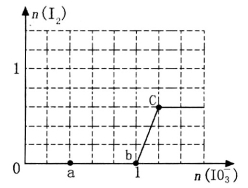
试回答下列问题:
(1)写出a点反应的离子方程式____________;反应中还原剂是_______;被还原的元素是________。
(2)写出b点到c点反应的离子方程式_______________。
(3)若往100mL 1 mol·L-1的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源:2015届山东省泰安市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列解释事实的化学方程式或离子方程式正确的是
A.用食醋除去暖水瓶中的水垢:2CH3COOH+CaCO3═Ca2++2CH3COO-+CO2↑+H2O
B.碳酸氢铵溶液中加入足量氢氧化钡溶液:NH4++HCO3—+2OH—═CO32-+NH3 H2O+H2O
H2O+H2O
C.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2
D.Ca(HCO3)2溶液中加入少量的NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+ CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源:2015届山东省泰安市高三上学期期中考试化学试卷(解析版) 题型:选择题
分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是
A.H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物
B.HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸
C.HF、CH3CH2OH、NaOH都易溶于水,都是电解质
D.HClO、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第一次(10月)检测化学试卷(解析版) 题型:填空题
(8分) NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI===2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是________。
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有________(填序号)。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是________(填编号)。
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)若反应10Al+6NaNO3+4NaOH===10NaAlO2+3N2↑+2H2O转移5 mol e-,则生成标准状况下N2的体积为________L。
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第一次(10月)检测化学试卷(解析版) 题型:选择题
下列关于实验操作的说法正确的是 ( )
A.可用25 mL碱式滴定管量取20.00 mL KMnO4溶液
B.用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
C.蒸馏时蒸馏烧瓶中液体的体积不能超过容积的2/3,液体也不能蒸干
D.将金属钠在研钵中研成粉末,使钠与水反应的实验更安全
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三第一次学情调查化学试卷(解析版) 题型:选择题
反应:L(s)+aG(g) bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。
bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。
据此可判断

A.上述反应是放热反应 B.上述反应是吸热反应
C.a>b D.无法判断a,b大小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com