
ijĪĀ¶ČĻĀŌŚČŻ»żĪŖ 2L µÄĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦ 2X(g) + Y(g)  2W(g)£»”÷H£¼0£¬µ±³äČė 2 mol X ŗĶ 1 mol Y£¬¾20 s“ļµ½Ę½ŗāŹ±Éś³ÉĮĖ 0.4 molW”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø£©
2W(g)£»”÷H£¼0£¬µ±³äČė 2 mol X ŗĶ 1 mol Y£¬¾20 s“ļµ½Ę½ŗāŹ±Éś³ÉĮĖ 0.4 molW”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø£©
¢ŁÉżøßĪĀ¶Č£¬W µÄĢå»ż·ÖŹż¼õŠ”£¬”÷H Ōö“ó
¢ŚŅŌ Y µÄÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ 0.01 mol/(L·s)
¢ŪŌŚĘäĖüĢõ¼ž²»±äµÄĒéæöĻĀ£¬Ōö¼Ó 1 mol X £¬Ōņ X ŗĶ Y µÄ×Ŗ»ÆĀŹ¾łĢįøß
¢ÜŌö“óŃ¹Ēæ£¬Õż·“Ó¦ĖŁĀŹŌö“ó£¬Äę·“Ó¦ĖŁĀŹ¼õŠ”£¬ŌņĘ½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆ
¢ŻŌŁĻņČŻĘ÷ÖŠĶØČė 2 mol X ŗĶ 1 mol Y£¬“ļµ½Ę½ŗāŹ±£¬X”¢Y µÄ×Ŗ»ÆĀŹ¾łŌö“ó”£
A”¢¢Ł¢Ż B”¢¢Ż C”¢¢Ś¢Ū¢Ü D”¢¢Ü¢Ż
”¾ÖŖŹ¶µć”æ»Æѧ·“Ó¦ĖŁĀŹÓė»ÆŃ§Ę½ŗā G1 G2
”¾“š°ø½āĪö”æB½āĪö£ŗÉżøßĪĀ¶Č£¬WµÄĢå»ż·ÖŹż¼õŠ”£¬ŌņĘ½ŗāÄęĻņŅĘ¶Æ£¬µ«”÷H²»±ä£¬ŅņĪŖ”÷HÓė·½³ĢŹ½µÄŠ“·ØÓŠ¹Ų£¬·½³ĢŹ½Č·¶Ø£¬”÷HČ·¶Ø£¬¢Ł“ķĪó£» ÓĆWµÄÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹv=0.4mol/2L·20s=0.01mol/£ØL•s£©£¬ĖłŅŌÓĆY±ķŹ¾µÄ·“Ó¦ĖŁĀŹ0.005 mol/£ØL•s£©£¬¢Ś“ķĪó£»Ōö¼ÓXµÄĮæ£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬ŌņXµÄ×Ŗ»ÆĀŹ»į¼õŠ”£¬YµÄ×Ŗ»ÆĀŹŌö“󣬢Ū“ķĪó£»Ōö“óŃ¹Ēæ£¬ÕżÄę·“Ó¦ĖŁĀŹ¶¼¼Óæģ£¬Ę½ŗāĻņĘųĢåĢå»ż¼õŠ”µÄ·½ĻņŅĘ¶Æ£¬¼“Ļņ×ÅÕż·“Ó¦·½ĻņŅĘ¶Æ£¬¢Ü“ķĪó£»ŌŁĻņČŻĘ÷ÖŠĶØČė 2 mol X ŗĶ 1 mol Y£¬Ļąµ±ŹĒ¶ŌŌĘ½ŗā¼ÓŃ¹£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬“ļµ½Ę½ŗāŹ±£¬X”¢Y µÄ×Ŗ»ÆĀŹ¾łŌö“󣬢ŻÕżČ·”£Ń”B”£
”¾Ė¼Ā·µć²¦”æĘ½ŗā·¢ÉśŅĘ¶Æ£¬²»ÄÜĖµ·“Ó¦ČČ·¢Éś±ä»Æ£¬·“Ó¦ČČÖ»Óė·½³ĢŹ½µÄŠ“·ØÓŠ¹Ų”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £©
A.ĆæŅ»ÖÜĘŚµÄŌŖĖŲ¶¼ŹĒ“Ó¼ī½šŹōæŖŹ¼£¬×īŗóŅŌĻ”ÓŠĘųĢå½įŹų
B.Ķ¬Ņ»ÖÜĘŚÖŠ(³żµŚŅ»ÖÜĘŚĶā)£¬“Ó×óµ½ÓŅ£¬ø÷ŌŖĖŲŌ×ÓŗĖµÄµē×ÓŹż¶¼ŹĒ“Ó1øöÖš½„Ōö¼Óµ½8øö
C.µŚ¶ž”¢ČżÖÜĘŚÉĻĻĀĻąĮŚŌŖĖŲµÄŌ×ÓŗĖĶāµē×ÓŹżĻą²ī8øö
D.µŚĘßÖÜĘŚÖ»ÓŠ23ÖÖŌŖĖŲ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
)Į×ĖįČ¼ĮĻµē³ŲŹĒÄæĒ°½ĻĪŖ³ÉŹģµÄČ¼ĮĻµē³Ų£¬Ę仳±¾×é³ÉŗĶ·“Ó¦ŌĄķČēĻĀ”£
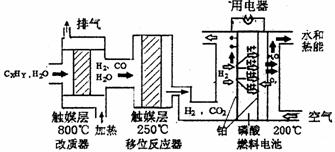
£Ø1£©ŌŚøÄÖŹĘ÷ÖŠÖ÷ŅŖ·¢ÉśµÄ·“Ó¦ĪŖ_______________________________
£Ø2£©ŅĘĪ»·“Ó¦Ę÷ÖŠCO(g)+H2O (g) 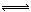 CO2 (g)+H2(g) £¬ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬ŌŚ1LČŻĘ÷ÖŠ·¢ÉśÉĻŹö·“Ó¦£¬ø÷ĪļÖŹµÄĪļÖŹµÄĮæÅØ¶Č±ä»ÆČēĻĀ±ķ£ŗ
CO2 (g)+H2(g) £¬ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬ŌŚ1LČŻĘ÷ÖŠ·¢ÉśÉĻŹö·“Ó¦£¬ø÷ĪļÖŹµÄĪļÖŹµÄĮæÅØ¶Č±ä»ÆČēĻĀ±ķ£ŗ
| t/min | COmol/L) | H2O(mol/L) | CO2(mol/L) | H2(mol/L) |
| 0 | 0.2 | 0.3 | 0 | 0 |
| 2 | n1 | n2 | n3 | 0.1 |
| 3 | n1 | n2 | n3 | 0.1 |
| 4 | 0.09 | 0.19 | 0.11 | 0.11 |
¢Ł“ĖĪĀ¶ČĻĀ£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ________
¢Ś·“Ó¦ŌŚ3”«4 minÖ®¼ä£¬ĒāĘųµÄĪļÖŹµÄĮæŌö¶ąµÄŌŅņæÉÄÜŹĒ £ØĢī“śŗÅ£©
A£®³äČėĖ®ÕōĘū B£®ÉżøßĪĀ¶Č C£®Ź¹ÓĆ“ß»Æ¼Į D£®³äČėĒāĘų
£Ø3£©Į×ĖįČ¼ĮĻµē³Ųøŗ¼«ÅųöµÄĘųĢåÖ÷ŅŖŹĒ___ __£¬
øƵē³ŲÕż¼«µÄµē¼«·“Ó¦ĪŖ_ _ __”£
£Ø4£©Į×ĖįČ¼ĮĻµē³ŲµÄµē¼«ÉĻ¶ĘĮĖ²¬·Ū£¬ÕāŃł×öµÄÄæµÄ£¬³żĮĖĘšµ½øüŗƵĵ¼µē×÷ÓĆĶā£¬»¹¾ß±øµÄ×÷ÓĆŹĒ ”£
£Ø5£©×ÜĢåæ“Ą“£¬ÕūøöĢåĻµÖŠÄÜĮæĄ“×ŌÓėCxHyÓėæÕĘųµÄ·“Ó¦£¬¼ŁÉčCxHyĪŖŠĮĶ飬ĒŅ
ŅŃÖŖŠĮĶéµÄČ¼ÉÕČČĪŖ5 518 kJ·mol£1£¬ĒėŠ“³öŠĮĶéČ¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ņ»¶ØĪĀ¶ČĻĀ£¬ŌŚČżøöĢå»ż¾łĪŖ1.0LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗ2CH3OH(g) CH3OCH3(g)£«H2O(g)£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £Ø £©
CH3OCH3(g)£«H2O(g)£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £Ø £©
| ČŻĘ÷ ±ąŗÅ | ĪĀ¶Č£Ø”ę£© | ĘšŹ¼ĪļÖŹµÄĮæ£Ømol£© | Ę½ŗāĪļÖŹµÄĮæ£Ømol£© | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| I | 387 | 0.20 | 0.080 | 0.080 |
| ¢ņ | 387 | 0.40 | ||
| ¢ó | 207 | 0.20 | 0.090 | 0.090 |
A”¢øĆ·“Ó¦µÄÕż·½ĻņÓ¦ĪŖĪüČČ·“Ó¦
B£®“ļµ½Ę½ŗāŹ±£¬ČŻĘ÷IÖŠµÄCH3OHĢå»ż·ÖŹż±ČČŻĘ÷¢ņµÄŠ”
C£®ČŻĘ÷IÖŠ·“Ó¦“ļµ½Ę½ŗāĖłŠčŹ±¼ä±ČČŻĘ÷¢óÖŠµÄ³¤
D£®ČōĘšŹ¼Ź±ĻņČŻĘ÷IÖŠ³äČėCH3OH 0.1mol”¢CH3OCH3 0.15molŗĶH2O 0.10mol£¬Ōņ·“Ó¦½«ĻņÕż·“Ó¦·½Ļņ½ųŠŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
SiCl4ŌŚŹŅĪĀĻĀĪŖĪŽÉ«ŅŗĢ壬Ņ×»Ó·¢£¬ÓŠĒæĮŅµÄ“Ģ¼¤ŠŌ”£°ŃSiCl4ĻČ×Ŗ»ÆĪŖSiHCl3£¬ŌŁ¾ĒāĘų»¹ŌÉś³Éøß“æ¹č”£Ņ»¶ØĢõ¼žĻĀ£¬ŌŚ20LŗćČŻĆܱÕČŻĘ÷ÖŠ·¢ÉśSiCl4×Ŗ»ÆĪŖSiHCl3 µÄ·“Ó¦£ŗ3SiCl4(g)£«2H2(g)£«Si(s) 4SiHCl3(g)””¦¤H£½Q kJ·mol£1”£2 minŗó“ļµ½Ę½ŗā£¬H2ÓėSiHCl3µÄĪļÖŹµÄĮæÅØ¶Č·Ö±šĪŖ0.1 mol·L£1ŗĶ0.2 mol·L£1”£
4SiHCl3(g)””¦¤H£½Q kJ·mol£1”£2 minŗó“ļµ½Ę½ŗā£¬H2ÓėSiHCl3µÄĪļÖŹµÄĮæÅØ¶Č·Ö±šĪŖ0.1 mol·L£1ŗĶ0.2 mol·L£1”£
£Ø1£©“Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬v(SiCl4)£½ ”£
£Ø2£©øĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK£½ £¬ĪĀ¶ČÉżøߣ¬KÖµŌö“ó£¬ŌņQ 0(Ģī”°£¾”±”¢”°£¼”±»ņ”°£½”±)”£
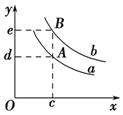 £Ø3£©ČōĘ½ŗāŗóŌŁĻņČŻĘ÷ÖŠ³äČėÓėĘšŹ¼Ź±µČĮæµÄSiCl4ŗĶH2(¼ŁÉčSi×ćĮæ)£¬µ±·“Ó¦ŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬ÓėŌĘ½ŗāĻą±Č½Ļ£¬H2µÄĢå»ż·ÖŹż½« (Ģī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±)”£
£Ø3£©ČōĘ½ŗāŗóŌŁĻņČŻĘ÷ÖŠ³äČėÓėĘšŹ¼Ź±µČĮæµÄSiCl4ŗĶH2(¼ŁÉčSi×ćĮæ)£¬µ±·“Ó¦ŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬ÓėŌĘ½ŗāĻą±Č½Ļ£¬H2µÄĢå»ż·ÖŹż½« (Ģī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±)”£
£Ø4£©ŌČŻĘ÷ÖŠ£¬ĶØČėH2µÄĢå»ż(±ź×¼×“æöĻĀ)ĪŖ ”£
£Ø5£©Ę½ŗāŗ󣬽«ČŻĘ÷µÄĢå»żĖõĪŖ10 L£¬ŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬
H2µÄĪļÖŹµÄĮæÅØ¶Č·¶Ī§ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŌĮņĖįĶČÜŅŗ×÷µē½āŅŗ£¬¶Ōŗ¬ÓŠŌÓÖŹFe”¢Zn”¢AgµÄ“ÖĶ½ųŠŠµē½ā¾«Į¶£®ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø””””£©
¢Ł“ÖĶÓėÖ±Į÷µēŌ“øŗ¼«ĻąĮ¬
¢ŚŅõ¼«·¢ÉśµÄ·“Ó¦ĪŖCu2£«£«2e£===Cu
¢ŪµēĀ·ÖŠĆæĶعż3£®01”Į1023øöµē×Ó£¬µĆµ½µÄ¾«ĶÖŹĮæĪŖ16 g
¢ÜŌÓÖŹAgŅŌAg2SO4µÄŠĪŹ½³ĮČėµē½ā²ŪŠĪ³ÉŃō¼«Äą
A£®¢Ł¢Ū”””” B£®¢Ś¢Ü C£®¢Ū¢Ü D£®¢Ś¢Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÄųļÓ£ØNi£Cd£©æɳäµēµē³ŲŌŚĻÖ“śÉś»īÖŠÓŠ¹ć·ŗÓ¦ÓĆ£®ŅŃÖŖijÄųļÓµē³ŲµÄµē½āÖŹČÜŅŗĪŖKOHČÜŅŗ£¬Ęä³ä”¢·Åµē°“ĻĀŹ½½ųŠŠ£ŗ
Cd£«2NiOOH£«2H2O Cd£ØOH£©2£«2Ni£ØOH£©2
Cd£ØOH£©2£«2Ni£ØOH£©2
ÓŠ¹ŲøƵē³ŲµÄĖµ·Ø²»ÕżČ·µÄŹĒ £Ø””””£©
A£®·ÅµēŹ±»ÆѧÄܲ»ÄÜČ«²æ×Ŗ»ÆĪŖµēÄÜ
B£®·ÅµēŹ±CdĪŖøƵē³ŲµÄøŗ¼«£¬³äµēŹ±ÕāŅ»¶ĖÓ¦½ÓÖ±Į÷µēŌ“µÄÕż¼«
C£®·ÅµēŹ±øƵē³ŲµÄÕż¼«·“Ó¦ĪŖ£ŗNiOOH£«H2O£«e£===Ni£ØOH£©2£«OH£
D£®³äµēŹ±£¬Ņõ¼«·“Ó¦ĪŖ£ŗCd£ØOH£©2£«2e£===Cd£«2OH£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖŌŚ25”ꏱ£¬FeS”¢CuSµÄČܶȻż³£Źż£ØKsp£©·Ö±šĪŖ6£®3”Į10£18”¢1£®3”Į10£36£®³£ĪĀŹ±ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ £Ø””””£©
A£®ĻņH2SµÄ±„ŗĶČÜŅŗÖŠĶØČėÉŁĮæSO2ĘųĢåČÜŅŗµÄĖįŠŌŌöĒæ
B£®½«×ćĮæµÄCuSO4ČܽāŌŚ0£®1 mol/LµÄH2SČÜŅŗÖŠ£¬ČÜŅŗÖŠCu2£«µÄ×ī“óÅضČĪŖ1£®3”Į10£35 mol/L
C£®ŅņĪŖH2SO4ŹĒĒæĖį£¬ĖłŅŌ·“Ó¦£ŗCuSO4£«H2S===CuS”ż£«H2SO4²»ÄÜ·¢Éś
D£®³żČ„¹¤Ņµ·ĻĖ®ÖŠµÄCu2£«æÉŅŌŃ”ÓĆFeS×÷³Įµķ¼Į
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠČżøöŹż¾Ż£ŗ¢Ł7.2”Į10﹣4”¢¢Ś2.6”Į10﹣4”¢¢Ū4.9”Į10﹣10·Ö±šŹĒČżÖÖĖįµÄµēĄėĘ½ŗā³£Źż£¬ČōŅŃÖŖÕāŠ©ĖįæÉŅŌ·¢ÉśČēĻĀ·“Ó¦£ŗNaCN+HNO2=HCN+NaNO2”” NaCN+HF=HCN+NaF NaNO2+HF=HNO2+NaF ÓÉ“ĖæÉÅŠ¶ĻĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | HNO2µÄµēĄėĘ½ŗā³£ŹżŹĒ¢Ū | B£® | HNO2µÄµēĄėĘ½ŗā³£ŹżŹĒ¢Ł |
| ”” | C£® | HCNµÄµēĄėĘ½ŗā³£ŹżŹĒ¢Ś | D£® | HFµÄµēĄėĘ½ŗā³£ŹżŹĒ¢Ł |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com