
【题目】现有含Na2O杂质的Na2O2试样,某同学欲测定Na2O2试样的纯度.回答下列问题 
(1)请从图①~⑦中选用适当的装置,其连接顺序为(填各接口的字母) .
(2)写出该实验中发生反应的化学方程式 .
(3)本实验中测量气体体积时主要应注意的事项有 .
(4)若实验时称取的试样为ag,产生的气体在标准状况下的体积为VmL,此试样中Na2O2的质量分数为 .
【答案】
(1)C接E,D接I
(2)2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH
(3)读数时气体要冷却到室温、量筒中液面的高度与集气瓶中液面的高度相同
(4)![]() %
%
【解析】解:(1)含Na2O杂质的Na2O2试样,欲测定Na2O2试样的纯度,根据题中提供的装置可知,该实验利用氧化钠和过氧化钠与水反应,该反应不需要不加热,其中过氧化钠与水反应产生氧气,称取一定量的样品,使其与水反应,根据产生的氧气的体积可计算出过氧化钠的质量,进而确定过氧化钠的质量分数,本实验中测量气体的体积是用排水量气法,所以实验装置的连接顺序为C接E,D接I,所以答案是:C接E,D接I;(2)实验中氧化钠和过氧化钠均能和水反应,方程式为:2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH,
所以答案是:2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH;(3)由于过氧化钠与水反应是放热反应,为了准确测量气体的体积,要使气体的温度与室温相同,所以测量气体时要冷却到室温,同时也要使集气瓶中的压强与大气压相同,所以在读数时,注意量筒中液面的高度与集气瓶中液面的高度相同,
所以答案是:读数时气体要冷却到室温、量筒中液面的高度与集气瓶中液面的高度相同;(4)根据反应2Na2O2+2CO2=2Na2CO3+O2 , 反应结束后测得气体体积为VmL(标准状况),即生成的氧气的物质的量为 ![]() mol,过氧化钠的物质的量为
mol,过氧化钠的物质的量为 ![]() ×2mol,
×2mol,
过氧化钠的纯度= ![]() ×100%=
×100%= ![]() %,
%,
所以答案是: ![]() %.
%.


 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案科目:高中化学 来源: 题型:
【题目】2016年3月10日,中科院上海光机所强场激光物理重点实验室宣布,其利用超强短激光成功产生反物质,这是我国科学家首次利用激光成功产生反物质.物质和反物质是对称的,反物质是由反粒子构成,反粒子的质量、寿命、自旋等与粒子完全相同,但所带电荷的电性相反.如果用反质子和反中子代替原子核中的质子和中子,就得到反原子核,再配以正电子,就形成反原子,反原子构成反分子,进而构成反物质.下列选项错误的是( )
A.氢原子的结构示意图为: ![]() ;则反氢原子的结构示意图为:
;则反氢原子的结构示意图为: ![]()
B.反氢原子中有一个带负电荷的反质子和一个带正电荷的反电子
C.反氢原子的摩尔质量为1g/mol
D.21H的反氢原子中有2个带负电荷的反质子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M的名称是乙烯雌酚,它是一种激素类药物,结构简式如图.下列叙述不正确的是( ) 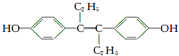
A.M的分子式为C18H20O2
B.1 mol M与饱和溴水混合,最多消耗5 mol Br2
C.1 mol M最多能与7 mol H2发生加成反应
D.M与NaOH溶液或NaHCO3溶液均能反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,①~⑦均为中学化学常用的实验装置. 
(1)若用图①装置制备氨气,写出化学方程式 .
(2)利用图②装置,在实验室可制备下列哪些气体(填字母代号).
a.C2H4 b.NO2 c.H2 d.Cl2 e.CO2 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯的原子序数为17,35Cl是氯的一种同位素,下列说法正确的是( )
A.35Cl原子所含质子数为18
B.![]() mol的1H35Cl分子所含中子数约为6.02×1023
mol的1H35Cl分子所含中子数约为6.02×1023
C.3.5g35Cl2气体的体积约为22.4L
D.35Cl2气体的摩尔质量为70
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 1 mol H2O的质量为18g/mol
B. CH4的摩尔质量为16g
C. 3.01×1023个SO2分子的质量为32g
D. 标准状况下,1 mol任何物质体积均为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1所示:向饱和Ba(OH)2溶液中逐滴加入稀硫酸,不断搅拌至过量. 
(1)主要的实验现象:烧杯中 , 灯泡 .
(2)烧杯中反应的离子方程式: .
(3)图2所示能正确表示实验过程的是(填序号).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com