
设NA代表阿伏加德罗常数的数值,下列说法正确的是
A.12.4 g白磷中含有共价键数为0.4 NA
B.3Fe+4H2O(g)  Fe3O4+4H2反应中,当5.6 g Fe全部转化为Fe3O4时,则有0.3 NA电子发生转移
Fe3O4+4H2反应中,当5.6 g Fe全部转化为Fe3O4时,则有0.3 NA电子发生转移
C.在1 L 0.1 mol/L碳酸钠溶液中阴离子总数等于0.1 NA
D.在标准状况下,22.4 L CH4与18 g H2O所含有的电子数均为10 NA
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:2014-2015广东省佛山市高一下学期第一次月考理化学试卷(解析版) 题型:选择题
用氯气给自来水消毒,某学生用自来水配制下列物质的溶液,药品不会产生明显变质的是
A.石蕊 B.硝酸银 C.亚硫酸钠 D.氯化铝
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市高三下学期第二次质量检测理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.12g金刚石晶体中含有的C—C的数目为2NA
B.1L 1 mol·L-1 AlCl3溶液中含有的Al3+数目为NA
C.在标况下,11.2L氯气通入足量的NaOH溶液中转移电子数为NA
D.18g重水(D2O)含有的中子数为10 NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市和平区高三下学期第一次质量调查化学试卷(解析版) 题型:选择题
在一定温度下,将等量的气体分别通入起始体积相同的密闭容器Ⅰ和Ⅱ中,使其发生反应,t0时容器Ⅰ中达到化学平衡,X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是
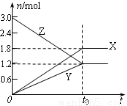
A.该反应的化学方程式为:3X+2Y 2Z
2Z
B.若两容器中均达到平衡时,两容器的体积V(Ⅰ)<V(Ⅱ),则容器Ⅱ达到平衡所需时间小于t0
C.若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态
D.若达平衡后,对容器Ⅱ升高温度时其体积增大,说明Z发生的反应为吸热反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省资阳市高三第三次模拟考试理综化学试卷(解析版) 题型:填空题
(15分)聚芳酯(PAR)是分子主链上带有苯环和酯基的特种工程塑料,在航空航天等领域具有广泛应用。下图是利用乙酰丙酸(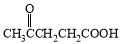 )合成聚芳酯E的路线:
)合成聚芳酯E的路线:
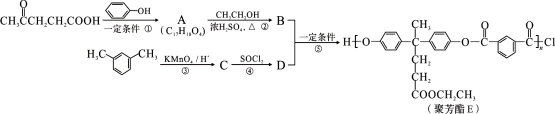
已知:①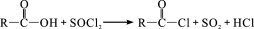
②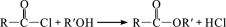 (R、R′表示烃基)
(R、R′表示烃基)
(1)乙酰丙酸中含有的官能团是羰基和 (填官能团名称)。
(2)D的结构简式为 。
(3)下列关于有机物B的说法正确的是 (填字母代号)。
a.能发生取代反应 b.能与浓溴水反应
c.能发生消去反应 d.能与H2发生加成反应
(4)A→B的化学方程式为 。
(5)C的分子式为 ,符合下列条件的C的同分异构体有 种。
①能发生银镜反应
②能与NaHCO3溶液反应
③分子中有苯环,分子中无 结构
结构
在上述同分异构体中,有一种苯环上有两个取代基且核磁共振氢谱图有4种峰的物质,写出该物质与足量NaOH溶液共热反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省渭南市高三教学质量检测(一模)化学试卷(解析版) 题型:填空题
(12分)(1)已知下列反应的热化学方程式为:
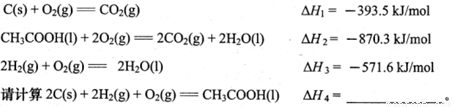
(2)某可逆反应在不同条件下的反应历程分别为A、B,如图所示。
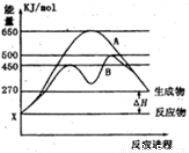
①据图判断该反应是_______(填“吸”或“放”)热反应,当反应达到平衡后,其他条件不变,降低温度,反应物的转化率_______(填“增大”、“减小”或“不变”);
②其中B历程农明此反应采用的条件为__________(选填序号)。
A.升高温度 B.增大反应物的浓度
C.降低温度 D.使用催化剂
(3)一定温度下,在3L容积可变的密闭容器中发生反应H2(g)+CO2(g) 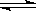 H2O (g)+CO(S),已知c(CO)与反应时间t变化曲线I如图所示,
H2O (g)+CO(S),已知c(CO)与反应时间t变化曲线I如图所示,
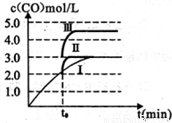
若在t0时刻分别改变一个条件,曲线I变为曲线II和曲线III。 当曲线I变为曲线II时,改变的条件是_______________。当曲线I变为曲线III时,改变的条件是________.
(4)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将0.2 mol/L的乙酸与0.1 mol/LNaOH溶液等体积混合后溶液显酸性,则混合溶液中离子浓度由大到小的顺序为_________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省渭南市高三教学质量检测(一模)化学试卷(解析版) 题型:选择题
儿茶素(其结构简式如图所示)是茶叶的主要活性成分,具有抗氧化、抗菌、除臭等作用。下列说法正确的是
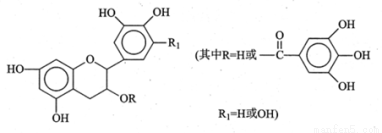
A.常温下,儿茶素不溶于水,也不溶于有机溶剂
B.儿茶素一定不能发生水解反应
C.儿茶素能与FeCl3溶液发生显色反应
D.1 mol儿茶素最少可与5mol NaOH反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市高三第一次模拟考试理综化学试卷(解析版) 题型:实验题
(15分)实验室常用苯甲醛在浓氢氧化钠溶液中制备苯甲醇和苯甲酸,反应如下:
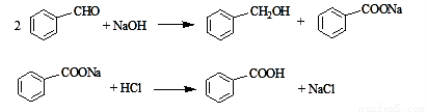
已知:①苯甲酸在水中的溶解度为:0.18 g(4 ℃)、0.34 g(25 ℃)、0.95 g(60 ℃)、6.8 g(95 ℃)。
②乙醚沸点34.6 ℃,密度0.7138,易燃烧,当空气中含量为1.83~48.0%时易发生爆炸。
③石蜡油沸点高于250 ℃
④苯甲醇沸点为205.3 ℃
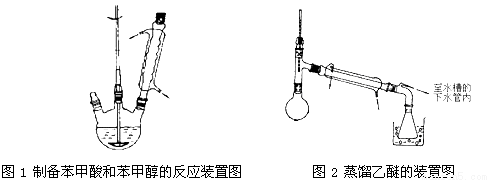
实验步骤如下:
①向图l所示装置中加入8 g氢氧化钠和30 mL水,搅拌溶解。稍冷,加入10 mL苯甲醛。开启搅拌器,调整转速,使搅拌平稳进行。加热回流约40 min。
②停止加热,从球形冷凝管上口缓缓加入冷水20 mL,摇动均匀,冷却至室温。然后用乙醚萃取三次,每次10 mL。水层保留待用。合并三次萃取液,依次用5 mL饱和亚硫酸氢钠溶液洗涤,10 mL 10%碳酸钠溶液洗涤,10 mL水洗涤,然后分液,将水层弃去,所得醚层进行实验步骤③。
③将分出的醚层,倒入干燥的锥形瓶中,加无水硫酸镁,注意锥形瓶上要加塞。将锥形瓶中溶液转入图2 所示的蒸馏装置,先缓缓加热,蒸出乙醚;蒸出乙醚后必须改变加热方式、冷凝方式,继续升高温度并收集205 ℃~206 ℃的馏分得产品A。
④将实验步骤②中保留待用的水层慢慢地加入到盛有30 mL浓盐酸和30 mL水的混合物中,同时用玻璃棒搅拌,析出白色固体。冷却,抽滤,得到粗产品,然后提纯得产品B。
根据以上步骤回答下列问题:
(1)步骤②萃取时用到的玻璃仪器除了烧杯、玻璃棒外,还需 (仪器名称)。
(2)步骤②中饱和亚硫酸氢钠溶液洗涤是为了除去 ,而用碳酸钠溶液洗涤是为了除去醚层中极少量的苯甲酸。醚层中少量的苯甲酸是从水层转移过来的,请用离子方程式说明其产生的原因 。
(3)步骤③中无水硫酸镁的作用是 ,锥形瓶上要加塞的原因是 ,产品A为 。
(4)步骤③中蒸馏除去乙醚的过程中采用的加热方式为 ;蒸馏得产品A的加热方式是 。
(5)步骤④中提纯产品B时所用到的实验方法为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高一下学期第一次月考化学试卷(解析版) 题型:选择题
元素X原子的最外层有6个电子,元素Y原子的最外层有3个电子,这两种元素形成的化合物的化学式可能是
A.X3Y2 B.X2Y C.Y2X3 D.Y3X2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com