
A.CH3OH B.NH3 C.H2O D.HF
科目:高中化学 来源: 题型:阅读理解
 A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | A | B | C | D |
| 性质 或 结构 信息 |
其单质和化合物的焰色均为黄色 | 其氢化物的水溶液能腐蚀玻璃 | 湿润的红色石蕊试纸遇其最低价氢化物变蓝 | 其原子核外有13种运动状态的电子 |


| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省菏泽市高三第二次模拟考试化学试卷(解析版) 题型:推断题
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物。
请回答下列问题:
(1)C、D、E三种原子对应的离子半径由大到小的顺序是 (填具体离子符号);由A、B、C三种元素按 4:2:3组成的化合物所含的化学键类型属于 。
(2)用某种废弃的金属易拉罐与 A、C、D组成的化合物溶液反应,该反应的离子方程式为: 。
(3)A、C两元素的单质与熔融K2CO3,组成的燃料电池,其负极反应式为 ,
用该电池电解1L1mol/LNaCl溶液,当消耗标准状况下1.12LA2时, NaCl溶液的PH= (假设电解过程中溶液的体积不变) 。
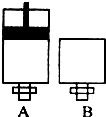
(4)可逆反应2EC2(气)+C2(气) 2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2 和2molEC2,使V (A ) = V (
B ) ,在相同温度下反应,则:① 达平衡所需时间:t(A ) t
( B )(填>、<、二,或:无法确定,下同)。平衡时 EC2 的转化率:a( A ) _a( B )。
2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2 和2molEC2,使V (A ) = V (
B ) ,在相同温度下反应,则:① 达平衡所需时间:t(A ) t
( B )(填>、<、二,或:无法确定,下同)。平衡时 EC2 的转化率:a( A ) _a( B )。

(5)欲比较C和E两元素的非金属性相对强弱,可采取的措施有 (填“序号”)。
a.比较这两种元素的气态氢化物的沸点
b.比较这两种元素的单质在常温下的状态
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的单质与氢气化合的难易
查看答案和解析>>
科目:高中化学 来源:09-10学年三明市五校高一下学期期中联考化学卷 题型:填空题
(15分)下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
|
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
|
1 |
A |
|
||||||
|
2 |
|
|
|
D |
E |
|
G |
|
|
3 |
B |
|
C |
J |
F |
|
H |
I |
(1)表中元素,化学性质最不活泼的是 ,只有负价而无正价的元素是 , 可用于制半导体材料的元素是_______
(2)C元素在元素周期表中的位置是 周期 族。
(3)最高价氧化物的水化物碱性最强的是 ,酸性最强的是 ,呈两性的是 ;
(4)A分别与E、G、H形成的化合物中,最稳定的 ;
(5)在B、C、E、F中,原子半径最大的是 .
(6)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式 。
(7)B、H两种元素形成的化合物所含的化学键类型为
(8)写出C的最高价氧化物与H的氢化物之间反应的离子方程式_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com