
科学家宣布发现了铝的“超级原子”结构———Al13和Al14。 已知这类“超级原子”最外层电子数之和为40个时处于相对稳定状态。下列说法中,正确的是
A.Al13、Al14互为同位素
B.Al13超原子中Al原子间通过离子键结合
C.Al14最外层电子数之和为42,与第ⅡA族元素原子的性质相似
D.Al13和Al14都具有较强的还原性,容易失去电子生成阳离子
科目:高中化学 来源:2016届浙江省富阳市高三上学期第二次质量检测化学试卷(解析版) 题型:选择题
在一定条件下,A、B、C、D之间可发生如下转化关系:A+B→C+D+H2O(未配平),且该过程为非氧化还原反应,则气体C不可能是
A.NH3 B.CO2 C.SO2 D.NO2
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期第一次月考化学试卷(解析版) 题型:简答题
(9分)高铁酸钠是一种高效多功能水处理剂。工业上常采用NaClO氧化法生产,反应原理为:在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4,过滤得到粗产品,再用NaOH溶液溶解,重结晶,用有机溶剂脱碱,低温烘干得到固体样品。反应方程式为:
3NaClO + 2Fe(NO3)3 + 10NaOH=2Na2FeO4↓+ 3NaCl + 6NaNO3 + 5H2O
(1)上述制备过程中,用NaOH溶液溶解粗产品而不用水的原因是 。
(2)高铁酸钠电池是一种新型可充电电池,电解质为NaOH溶液,放电时负极材料为Zn,正极产生红褐色沉淀,写出该电池反应方程式 。
(3)生产高铁酸钠的原料之一Fe(NO3)3用黑色粉末Fe(含有Fe3O4)与稀硝酸反应制备。准确称取该黑色粉末13.12g,加入200mL 4 mol·L-1 HNO3搅拌,固体完全溶解,共收集到标准状况下2688mL的气体,经分析其中只含有NO,并测得此时溶液中c(H+)=0.4mol·L-1(设反应前后溶液体积不变)。通过以上数据,计算该黑色粉末中Fe的质量分数。(写出计算过程,结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源:2016届河北省冀州市高三复习班上第一次月考化学试卷A(解析版) 题型:实验题
(10分)已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;
Mg和Na的化学性质也具有一定相似性。
I、用如图所示装置进行Mg与SO2反应的实验。

(1)选择制取SO2的合适试剂____________。
①10%的H2SO4溶液 ②70%的H2SO4溶液 ③Na2SO3固体 ④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式___________。
装置C中NaOH溶液的作用是______________。
(3)该装置仍有不足之处,请说明_______________。
Ⅱ、某研究小组进行了“实验室制Si”的研究,它们以课本为基础,查阅资料得到以下可供参考的四条信息:
①Mg在加热的条件下即可与SiO2反应
②金属硅化物与稀H2SO4反应生成硫酸盐与SiH4
③Si和SiO2均不与稀H2SO4反应
④SiH4在空气中自燃
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥;最后称量……在用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”。
(4)该小组“实验室制Si”的化学方程式是 。
(5)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是(用化学方程式说明): 。
查看答案和解析>>
科目:高中化学 来源:2016届河北省冀州市高三复习班上第一次月考化学试卷A(解析版) 题型:选择题
关于FeCl3进行的实验,下列预测正确的是
A.蒸发FeCl3溶液,得到FeCl3固体
B.在FeCl3、CuCl2混合液中,加入少量Fe粉,一定有H2产生且有Cu析出
C.用FeCl3固体溶于水配制饱和溶液,会有Fe(OH)3沉淀产生
D.在FeCl3溶液中,加入KHCO3溶液,有CO2产生,但无Fe(OH)3沉淀生成
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期二调化学试卷(解析版) 题型:实验题
(10分)资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2SO3。某化学兴趣小
组进行该实验时,却检测到生成的盐中含有SO42-。
(1)兴趣小组同学认为,上述反应的生成物可能与反应温度(T),KOH溶液的浓度(c)有关。他们做了如下对比实验(每次实验中硫粉的质量、KOH溶液的体积均相同)。

实验①~④是探究温度对生成物的影响,⑤~⑧是探究KOH溶液的浓度对生成物的影响。请在表中相应空格内填人相应数据。
(2)兴趣小组设计实验对上述反应中生成的盐的成分进行探究。他们提出如下假设,请你根据氧化还原反应的规律,完成假设二和假设三:
假设一:生成的盐是K2S和K2 S03;
假设二:生成的盐是____;
假设三:生成的盐是____;
(3)请你设计实验验证上述假设一。完成下表中内容。[除了硫粉与热的KOH溶液的反应液之外,可供选择的药品有稀硝酸,稀盐酸等;已知:6H++SO32-+2S2-=3S+3H2O
(4)兴趣小组通过改变硫粉的质量,得出生成钾盐的质量与硫粉质量的变化关系如图所示。有人据此得出结论:生成的盐一定是K2S和K2SO3的混合物。请你根据计算结果指出该结论是否正确 。
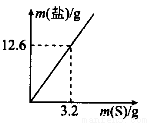
(5)请分析上述反应中有K2S04生成的可能原因是 。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期二调化学试卷(解析版) 题型:选择题
根据下图海水综合利用的工业流程图,判断下列说法正确的是
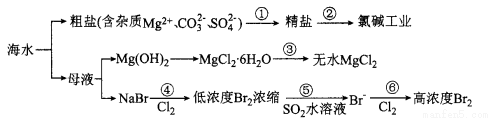
已知:MgCl2.6H20受热生成Mg(OH) Cl和HC1气体等。
A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质
B.在过程③中将MgCl2.6H20灼烧即可制得无水MgCl2
C.在过程④、⑥反应中每氧化0.2 mol Br一需消耗2.24LCl2
D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
查看答案和解析>>
科目:高中化学 来源:2016届安徽省合肥市高三上第二次段考化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数,下列说法不正确的是
A.含1 mol FeCl3的饱和溶液最多可形成胶体粒子数为NA
B.4.6 g Na与稀盐酸反应,转移电子数一定为0.2NA
C.10.6 g Na2 C03晶体中含CO32一数目为0.1 NA
D.常温下,22 g CO2含碳氧双键数目为NA
查看答案和解析>>
科目:高中化学 来源:2016届河北省衡水市高三复习班上月考化学试卷(解析版) 题型:选择题
下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍。下列说法正确的是

A.X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增
B.Y、Z、W元素在自然界中均不能以游离态存在, 它们的最高价氧化物的水化物的酸性依次递增
它们的最高价氧化物的水化物的酸性依次递增
C.YX2晶体熔化、液态WX3气化均需克服分子间作用力
D.根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com