
【题目】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
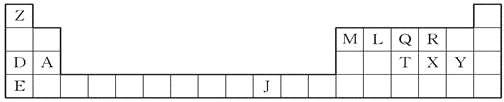
(1)T、X、Y原子的第一电离能由小到大的顺序是____________(用元素符号表示)。
(2)LX2分子的电子式是________________,XY2分子是____________(填“极性分子”或“非极性分子”);QY3分子中Q采用________杂化。
(3)由J、L、R三种元素形成的某种配位化合物,该化合物具有挥发性,化学式J(LR)4,其中J的化合价是0价。则基态J原子的核外电子排布式是___________________________;写出与配位体微粒互为等电子体的离子、分子各一种________、________。
(4)由Z、L、Q三种元素组成的化合物,分子式为Z9L3Q,它有_________种同分异构体(其中Q以三个单键与其他原子相连),请写出其中沸点最低的物质的结构简式__________________。
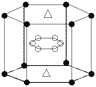
(5)A与M组成的一种化合物AM2,刷新了金属化合物超导温度的最高纪录。右图所示的是该化合物的晶体结构单元。图中上下底面中心“△”处的原子是________(填元素符号)。
【答案】(1)S<P<Cl (1分)(2)![]() 极性分子 sp3 (各1分)
极性分子 sp3 (各1分)
(3)1s22s22p63s23p63d84s2或[Ar]3d84s2CN-N2 (各1分)
(4) 4 N(CH3)3(2分) (5)Mg ( 2分)
【解析】试题分析:根据元素在周期表中的位置可判断A是Mg,D是Na,E是K,Z是H,M是B,L是C,Q是N,R 是O,T是P,X是S,Y是Cl,J是Ni。
(1)非金属性越强,第一电离能越大,但P元素的3p轨道电子处于半充满状态,稳定性强,第一电离能大于相邻元素,则T、X、Y原子的第一电离能由小到大的顺序是S<P<Cl。
(2)LX2分子是CS2,其结构与CO2类似,电子式![]() ,XY2分子SCl2,中心原子含有的价层电子对数是
,XY2分子SCl2,中心原子含有的价层电子对数是![]() ,含有2对孤对电子,其结构是V形,因此是极性分子;QY3分子是NCl3,中心原子含有的价层电子对数是
,含有2对孤对电子,其结构是V形,因此是极性分子;QY3分子是NCl3,中心原子含有的价层电子对数是![]() ,含有1对孤对电子,中Q采用sp3 杂化。
,含有1对孤对电子,中Q采用sp3 杂化。
(3)由J、L、R三种元素形成的某种配位化合物,该化合物具有挥发性,化学式Ni(CO)4,其中Ni的化合价是0价,原子序数是28,则根据核外电子排布规律可知基态J原子的核外电子排布式是1s22s22p63s23p63d84s2或[Ar]3d84s2;原子数和价电子数分别都相等的是等电子体,则与CO互为等电子体的离子、分子分别是CN-、N2。
(4)由Z、L、Q三种元素组成的化合物,分子式为Z9L3Q,结构简式有CH3CH2CH2NH2,CH3CH(NH2)CH3,HN(CH3)2,N(CH3)3,有4种同分异构体,其中支链越多,沸点越低,因此沸点最低的物质的结构简式为N(CH3)3。
(5)A与M组成的一种化合物MgB2,根据晶胞结构可知顶点处的原子共计有12×1/6=2,位于面上的原子共计是2×1/2=1,所以图中上下底面中心“△”处的原子是Mg。


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
【题目】电-Fenton法是用于水体里有机污染物降解的高级氧化技术。其反应原理如图所示,其中电解产生的H2O2与Fe2+发生Fenton反应:Fe2++H2O2![]() Fe3++OH- +·OH,生成的羟基自由基(·OH)能氧化降解有机污染物。下列说法不正确的是
Fe3++OH- +·OH,生成的羟基自由基(·OH)能氧化降解有机污染物。下列说法不正确的是
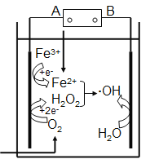
A.电源的A极是负极
B.电解池中只有O2、Fe3+发生还原反应
C.阳极上发生电极反应:H2O-e-![]() ·OH + H+
·OH + H+
D.消耗1molO2,可以产生4mol ·OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多沙唑嗪盐酸盐是一种用于治疗高血压的药物。多沙唑嗪的合成路线如下:
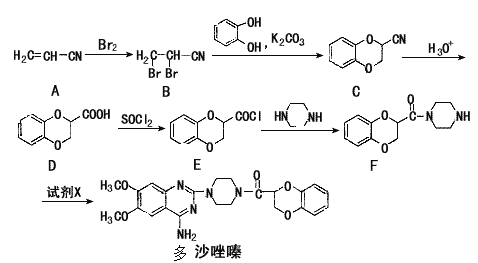
(1)写出D中两种含氧官能团的名称:______和_____。
(2)写出满足下列条件的D的两种同分异构体的结构简式_______________________。
①苯的衍生物,且苯环上的一取代产物只有两种;②与Na2CO3溶液反应放出气体;
③水解后的产物才能与FeCl3溶液发生显色反应。
(3)E→F的反应中还可能生成一种有机副产物,该副产物的结构简式为____________。
(4)由F制备多沙唑嗪的反应中要加入试剂X(C10H10N3O2Cl),X的结构简式为_______。
(5)苯乙酸乙酯是一种常见的合成香料。请设计合理的方案以苯甲醛和乙醇为原料合成
苯乙酸乙酯(用合成路线流程图表示,并注明反应条件)。
提示:①R-Br+Na→R-CN+NaBr;
②合成过程中无机试剂任选;
③合成路线流程图示例如下:
CH3CH2OH ![]() H2C=CH2
H2C=CH2![]() BrH2C-CH2Br
BrH2C-CH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3经一系列反应可以得到HNO3和NH4NO3,如下图所示。
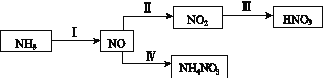
(1)Ⅰ中,NH3和O2在催化剂作用下反应,其化学方程式是______________。
(2)Ⅱ中,2NO(g)+O2(g)![]() 2NO2(g)。在其他条件相
2NO2(g)。在其他条件相
同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
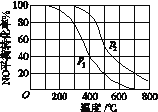
①比较p1、p2的大小关系:p1________p2(填“<”,“>”或“=”)
②随温度升高,该反应平衡常数变化的趋势是________(填“增大”,“减小”或“不变”)。
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
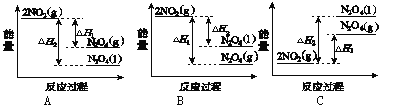
①已知:2NO2(g)![]() N2O4(g) ΔH12NO2(g)
N2O4(g) ΔH12NO2(g)![]() N2O4(l) ΔH2
N2O4(l) ΔH2
下列能量变化示意图中,正确的是(选填字母)________。
②N2O4与O2、H2O化合的化学方程式是____________________。
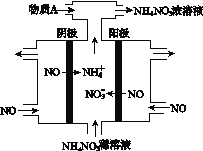
(4)Ⅳ中,电解NO制备NH4NO3,其工作原理如图所示。为使电解产物全部转化为NH4NO3,需补充A。A是______,说明理由:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子因发生氧化还原反应而不能大量共存的是( )
A.H+、Fe2+、NO3﹣、SO42﹣
B.Al3+、Na+、SO42﹣、HCO3﹣
C.Na+、Ca2+、Cl﹣、SO42﹣
D.Fe3+、K+、SCN﹣、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品干燥剂在食品加工、储存中应用非常广泛。食品干燥剂应无毒、无味、无腐蚀性及对环境友好。下列说法错误的是
A.硅胶可用作食品干燥剂
B.P2O5不可用作食品干燥
C.六水氯化钙可用作食品干燥剂
D.加工后具有吸水性的植物纤维可用作食品干燥剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是
A.胶体的丁达尔效应与微粒直径大小有关
B.氨气的水溶液能导电,因此是NH3电解质
C.电解质溶液的导电能力与溶液中离子浓度及离子所带电荷多少有关
D.向饱和氯化钠溶液中加入一小块钠,溶液中有固体析岀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或记录正确的是
A. 常温常压下测得1 mol N2的质量为28 g
B. 用量筒测得排水法收集制得的氢气的体积为50.28 mL
C. 用两只250 mL的容量瓶配制0.1 mol·L-1500 mL的NaOH溶液
D. 用托盘天平称得2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一些茶叶的包装盒中有一个小袋,将小袋打开可看到灰黑色粉末,其中有的已变成棕褐色。将这种灰黑色粉末投入稀盐酸后,取其上层清液并加几滴氯水,再滴加KSCN溶液,马上出现红色。以下结论不正确的是 ( )
A.该灰黑色粉末作抗氧化剂
B.该灰黑色粉末不可食用
C.小袋中原来装有铁粉
D.小袋中原来装有氧化铁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com