
| A. | Al | B. | Mg | ||
| C. | Na | D. | 三者产生的氢气一样多 |
 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 反应中B2O3是氧化剂 | B. | 若消耗2.24LNH3理论上可得2.5gBN | ||
| C. | 填料的作用可使反应物充分接触 | D. | 反应时NH3需要用无水CaCl2干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | UO3 | B. | UO2 | C. | 2UO2•UO3 | D. | UO2•2UO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到化学平衡时,5v正(O2)=4v逆(NO) | |
| B. | 若单位时间内生成nmol NO的同时,生成nmol NH3,则反应达到平衡状态 | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 | |
| D. | 化学反应速率关系是:2v正(NH3)=3v正(H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
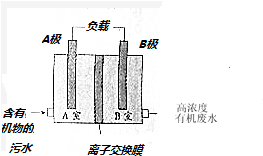
| A. | A极上发生类似C6H10O5-24e+7H2O═6CO2↑+24H+的电极反应 | |
| B. | B极上发生的是还原反应,工作过程中电极周围溶液的pH增大 | |
| C. | 工作过程中外电路的电子由A极流向B极,溶液中则由B极流向A极 | |
| D. | 污水中所存在的阳离子经离子交换膜由A室流向B室. |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 向电解质溶液中加入新物质时,其导电性符合如图所示变化趋势的实验操作是②.
向电解质溶液中加入新物质时,其导电性符合如图所示变化趋势的实验操作是②.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com