
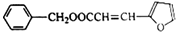 )的合成路线:
)的合成路线:

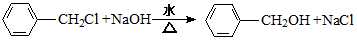 .A+D→E的反应类型为酯化反应.
.A+D→E的反应类型为酯化反应.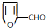 ,其最多有11个原子共平面.
,其最多有11个原子共平面. 与苯环相连;③能够发生水解反应④能够发生银镜反应.
与苯环相连;③能够发生水解反应④能够发生银镜反应.
分析 B是石油裂解的主要产物,其产量用于衡量化工发展的水平,则B为CH2=CH2,B和水发生加成反应生成C为CH3CH2OH,C被连续氧化生成D为CH3COOH,根据M结构简式知,C7H8为 ,甲苯发生甲基上的取代反应生成
,甲苯发生甲基上的取代反应生成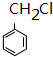 ,
, 发生水解反应生成A为
发生水解反应生成A为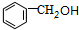 ,A和D发生酯化反应生成E为
,A和D发生酯化反应生成E为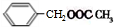 ,E发生信息②反应生成M,根据M结构简式知,F结构简式为
,E发生信息②反应生成M,根据M结构简式知,F结构简式为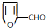 ,
,
(6)甲醇被催化氧化生成甲醛,乙酸和甲醇发生酯化反应生成乙酸甲酯,乙酸甲酯和甲醛发生取代反应生成丙烯酸甲酯,丙烯酸甲酯发生加聚反应生成聚丙烯酸甲酯,结合题目分析解答.
解答 解:(1)根据以上分析,E为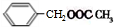 ,化学名称是乙酸苯甲酯,C结构简式为CH3CH2OH,官能团名称为羟基,故答案为:乙酸苯甲酯;羟基;
,化学名称是乙酸苯甲酯,C结构简式为CH3CH2OH,官能团名称为羟基,故答案为:乙酸苯甲酯;羟基;
(2)通过以上分析知,反应①为甲苯发生甲基上的取代反应生成 ,需要的条件是氯气、光照,故答案为:Cl2,光照;
,需要的条件是氯气、光照,故答案为:Cl2,光照;
(3)C7H7C1→A为 发生水解反应生成A为
发生水解反应生成A为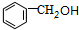 ,化学方程式为
,化学方程式为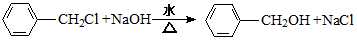 ,A和D发生酯化反应生成E为
,A和D发生酯化反应生成E为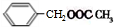 ,故答案为:
,故答案为: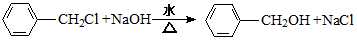 ;酯化反应;
;酯化反应;
(4)通过以上分析知,F结构简式为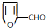 ,该分子中最多有11个原子共平面,故答案为:
,该分子中最多有11个原子共平面,故答案为: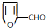 ;11;
;11;
(5)①属于苯的对位二取代衍生物,且与M具有相同官能团;② 与苯环相连;③能够发生水解反应④能够发生银镜反应,所以能够发生异构的为苯环上
与苯环相连;③能够发生水解反应④能够发生银镜反应,所以能够发生异构的为苯环上 的对位结构并且为甲酸酯,即HCOOCH=CH-CH2-,HCOOCH2-CH=CH-,
的对位结构并且为甲酸酯,即HCOOCH=CH-CH2-,HCOOCH2-CH=CH-,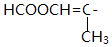
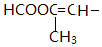
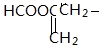
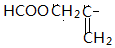

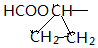 ,共8种,故答案为:8;
,共8种,故答案为:8;
(6)甲醇被催化氧化生成甲醛,乙酸和甲醇发生酯化反应生成乙酸甲酯,乙酸甲酯和甲醛发生取代反应生成丙烯酸甲酯,丙烯酸甲酯发生加聚反应生成聚丙烯酸甲酯,其合成路线为 ,故答案为:
,故答案为: .
.
点评 本题考查有机物推断和合成,为高频考点,侧重考查学生分析推断及知识迁移能力,明确反应条件、分子式、某些物质结构简式之间的关系是解本题关键,难点是同分异构体的判断以及合成路线设计,要求学生有扎实的基础扎实并灵活运用知识能力,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ③④⑤⑥ | C. | ②③④⑤ | D. | 全部都可以 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 乙酸乙酯是非常重要的有机溶剂和化工原料,如图转化关系中的①、②、③是工业上合成乙酸乙酯的常见反应,其中A是一种常见的调味品.请回答:
乙酸乙酯是非常重要的有机溶剂和化工原料,如图转化关系中的①、②、③是工业上合成乙酸乙酯的常见反应,其中A是一种常见的调味品.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,电子由石墨沿导线流向铝 | |
| B. | 放电时,正极反应式为:Al+Li++e-═AlLi | |
| C. | 充电时,铝电极质量增加 | |
| D. | 充电时,PF6-向阴极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4-、Cl- | Cl2、Mn2+ |
| A. | 第①组反应的其余产物为H2O和O2 | |
| B. | 第②组反应中参加反应的Cl2与FeBr2的物质的量之比为1:2 | |
| C. | 第③组反应中生成1molCl2,转移电子2mol | |
| D. | 氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
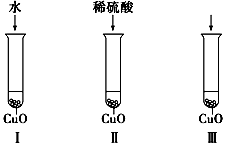 氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解.请你和他一起通过如图所示Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.
氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解.请你和他一起通过如图所示Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:HNO3>H3BO3>H2CO3 | B. | 稳定性:HF>PH3>H2O | ||
| C. | 碱性:Be(OH)2>Mg(OH)2>Ca(OH)2 | D. | 金属性:K>Mg>Al |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正丁烷分子储存的能量小于异丁烷 | |
| B. | 正丁烷的稳定性大于异丁烷 | |
| C. | 异丁烷转化为正丁烷的过程是一个放热过程 | |
| D. | 异丁烷转化为正丁烷的过程是一个吸热过程 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com