
 (a-xb)计算中心原子的孤对电子个数;
(a-xb)计算中心原子的孤对电子个数; (6-2×2)=3,该分子为V形结构,CO2的价层电子对个数=2+
(6-2×2)=3,该分子为V形结构,CO2的价层电子对个数=2+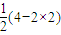 =2,该分子是直线形结构,故A错误;
=2,该分子是直线形结构,故A错误; (6-2×2)=1,CO2的孤电子对个数=
(6-2×2)=1,CO2的孤电子对个数=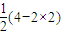 =0,所以二氧化硫有1对孤对电子,二氧化碳没有孤对电子,故C错误;
=0,所以二氧化硫有1对孤对电子,二氧化碳没有孤对电子,故C错误; (6-2×2)=3,该分子为V形结构,CO2的价层电子对个数=2+
(6-2×2)=3,该分子为V形结构,CO2的价层电子对个数=2+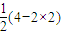 =2,该分子是直线形结构,故D正确;
=2,该分子是直线形结构,故D正确;

科目:高中化学 来源:2010年黑龙江省高二下学期期末考试化学试题 题型:选择题
对于SO2和CO2说法正确的是 ( )
A.都是直线形结构 B.中心原子都采用SP杂化轨道
C.S原子和C原子上都没有孤对电子 D.SO2为V形结构,CO2为直线形结构
查看答案和解析>>
科目:高中化学 来源:2012届山东省兖州市高二下学期期中考试化学试卷 题型:选择题
对于SO2和CO2说法正确的是
A. 都是直线形结构
B. 中心原子都采用sp杂化
C. S原子和C原子上都没有孤对电子
D. SO2为V形结构,CO2为直线形结构
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省泰州市兴化中学高二(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com