
下列关于0.10 mol·L-1 NaHCO3溶液的说法正确的是( )
A.溶质的电离方程式为NaHCO3===Na++H++CO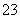
B.25 ℃时,加水稀释后,n(H+)与n(OH-)的乘积变大
C.离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO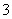 )+c(CO
)+c(CO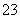 )
)
D.温度升高,c(HCO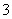 )增大
)增大
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
有甲、乙两容器,甲容器容积固定,乙容器容积可变。一定温度下,在甲中加入2 mol N2、3 mol H2,反应N2(g)+3H2(g)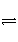
 2NH3(g)达到平衡时生成NH3的物质的量为m mol。
2NH3(g)达到平衡时生成NH3的物质的量为m mol。
(1)相同温度下,在乙中加入4 mol N2、6 mol H2,若乙的压强始终与甲的压强相等,乙中反应达到平衡时,生成NH3的物质的量为________mol(从下列各项中选择,只填序号,下同);若乙的容积与甲的容积始终相等,乙中反应达到平衡时,生成NH3的物质的量为________mol。
A.小于m B.等于m C.在m~2m之间 D.等于2m E.大于2m
(2)相同温度下,保持乙的容积为甲的一半,并加入1 mol NH3,要使乙中反应达到平衡时各物质的体积分数与上述甲容器中达到平衡时相同,则起始应加入______mol N2和________mol H2。
查看答案和解析>>
科目:高中化学 来源: 题型:
溶液的酸碱性和pH:
(1)25 ℃,0.01 mol·L-1的盐酸中,c(OH-)=________ mol·L-1,pH=____________,由水电离出的c(H+)=________。
(2)100 ℃时,pH=6的水中c(H+)=________ mol·L-1,该水显________性。
(3)100 ℃时(Kw=10-12),0.01 mol·L-1的NaOH溶液的pH为________________,由水电离出的c(OH-)=________。
(4)25 ℃时,pH=8的CH3COONa溶液中c(OH-)=__________________,由水电离的c(OH-)=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知Ba2+有很强的毒性,医学上进行消化系统的X射线透视时,常使用BaSO4作内服造影剂。胃酸酸性很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是______________________(用沉淀溶解平衡原理解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
化工生产中常用MnS作为沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)CuS(s)+Mn2+(aq),下列说法错误的是(双选)( )
A.MnS的Ksp比CuS的Ksp小
B.该反应达平衡时c(Mn2+)=c(Cu2+)
C.往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大
D.该反应的平衡常数K=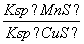
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下等物质的量浓度的下列溶液中,c(NH )最大的是( )
)最大的是( )
A.NH4Cl B.(NH4)2Fe(SO4)2
C.(NH4)2SO4 D.(NH4)2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:

某活动小组测定制取的Na2S2O3·5H2O的纯度的方法如下:准确称取W g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。反应原理为2S2O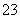 +I2===S4O
+I2===S4O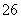 +2I-
+2I-
(5)滴定至终点时,溶液颜色的变化:____________________________________________。
(6)测定起始和终点的液面位置如图,则消耗碘的标准溶液体积为________mL。产品的纯度为(设Na2S2O3·5H2O相对分子质量为M)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学遍及人们的生活、工作和生产。下列说法不正确的是( )
A.合成氨工业中使用的氮气来自于空气
B.“地沟油”经加工处理后,可用于生产肥皂和生物柴油
C.亚硝酸钠是一种食品防腐剂,使用时其用量可以不加限制
D.利用合适的催化剂可以将机动车尾气中的CO和NO转化为无害物质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各图所示的现象或事实与胶体的性质无关的是( )

A.图①:日光下的树林
B.图②:长江三角洲的形成
C.图③:用激光笔照射氢氧化铁胶体
D.图④:钠的焰色反应实验
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com