
【题目】下列说法不正确的是
A.利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学方法
B.纤维素、淀粉、油脂均为天然高分子物质
C.通过红外光谱分析可以区分乙醇与乙酸乙酯
D.石油催化裂化的主要目的是提高汽油等轻质油的产量与质量;石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】(除标注外,其余每空1分,共7分)X、Y、Z、Q、R、T、U、W分别代表原子序数依次增大的前四周期元素。X和R属同族元素;Z和U位于第VIIA族;X和Z可形成化合物XZ4;Q基态原子的s轨道和p轨道的电子总数相等;T的一种单质在空气中能够自燃。W的外围电子排布式为3d63s2。
请回答下列问题:
(1)R基态原子的电子排布式是_________。W在元素周期表的位置是_____________。
(2)XU4的电子式是_____________,用一个离子方程式证明S(硫)元素和U元素的非金属性的强弱_____________。
(3)CuSO4溶液能用作T4中毒的解毒剂,反应可生成T的最高价含氧酸和铜,该反应的化学方程式是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在人体细胞中对生命活动起着重要作用,含量约占细胞鲜重总量97%的化学元素是
A. C、H、O、N、P、Ca B. C、H、O、N、P、K
C. C、H、O、N、S、K D. C、H、O、N、P、S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组对一含有Al3+的未知溶液进行分析:往该溶液逐滴滴加某浓度NaOH溶液,所加NaOH溶液体积(ml)与产生沉淀的物质的量(mol)的关系如下图所示:下列说法错误的是( )
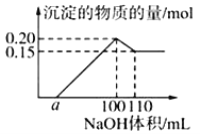
A.该未知溶液中至少含有3种阳离子
B.滴加的NaOH溶液的物质的量浓度为5 molL﹣1
C.若将最终沉淀过滤、洗涤、灼烧,其质量一定为6 g
D.若溶液中仅有两种金属阳离子,且另一种离子为二价阳离子,则a=10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。
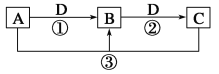
请回答下列问题:
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是_______________;用新型消毒剂ClO2代替A消毒的原因主要有
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,A与NaClO反应可得到肼(N2H4),该反应的化学方程式为________________________。
(3)若D是氯碱工业的主要产品之一,B有两性,则向C溶液滴加小苏打溶液反应的离子方程式是__________________。
(4)若A、C、D都是常见气体,C是导致酸雨的主要气体,写出A在酸性条件下和KMnO4反应溶液出现混浊的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H6)又称联氨,是一种可燃性的液体,可用作火箭燃料。
(1)101kPa,32.0g N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧的热化学方程式是:
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。肼—空气燃料电池放电时其负极的电极反应式是 。
(3)如右图是一个电化学过程示意图。
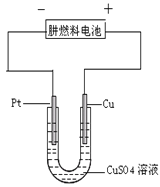
①铂片上发生的电极反应是 。
②假设使用肼—空气燃料电池作为本过程的电源,铜片质量变化128g,则肼—空气燃料电池理论上消耗标准状况下的空气 L(假设空气中氧气的体积含量为20%)。
(4)传统制备肼的方法是以NaClO氧化NH3制得肼的稀溶液,该反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由一分子含氮碱基、一分子磷酸和一分子化合物a构成了复杂化合物b,对a和b的准确叙述是
A. a是核糖,b则为核苷酸
B. a是脱氧核糖,b为脱氧核糖核酸
C. a是核糖,b为核糖核苷酸
D. a是五碳糖,b则为核苷酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[物质结构与性质]
将汽车尾气中含有的CO利用不仅能有效利用资源,还能防治空气污染。工业上常用CO与H2在由Al、Zn、Cu等元素形成的催化剂作用下合成甲醇。
(1)如图是某同学画出CO分子中氧原子的核外电子排布图:![]() ,请判断该排布图 (填“正确”或“错误”),理由是 (若判断正确,该空不用回答)。
,请判断该排布图 (填“正确”或“错误”),理由是 (若判断正确,该空不用回答)。
(2)写出与CO互为等电子体(电子总数相等)的一种分子和一种离子的化学式 。
(3)向CuSO4溶液中加入足量氨水可得到深蓝色[Cu(NH3)4]SO4溶液,[Cu(NH3)4]SO4中 所含配位键是通过配体分子的 给出孤电子对, 接受电子对形成,SO42-的空间构型是 ,该物质中N、O、S三种元素的第一电离能大小顺序为 > > (填元素符号)。
(4)甲醇与乙烷的相对分子质量相近,故二者分子间的作用力(范德华力)相近,但是二者沸点的差距却很大,造成该差异的原因是 ;在甲醇分子中碳原子轨道的杂化类型为 。
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图所示:

① 在该晶胞中,Cu+ 的配位数是 ,
② 若该晶胞的边长为a pm,则Cu2O的密度为________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol
B.1mol甲烷燃烧生成水蒸汽和二氧化碳所放出的热量是甲烷燃烧热
C.已知由石墨制备金刚石为吸热反应,则金刚石比石墨稳定
D.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com