
| A. | 5min时,v(C)=$\frac{x}{5}$Vmol•L-1•s-1 | |
| B. | 缩小容器体积平衡一定发生移动 | |
| C. | 0-5min内,v(A):v(C)=a:c | |
| D. | 0-5min内,用A表示的反应速率为$\frac{xc}{300aV}$mol•L-1•s-1 |
分析 A.化学反应速率是单位时间内的平均速率,不是瞬时速率,根据v=$\frac{\frac{△n}{V}}{△t}$计算v(C);
B.若反应气体气体分子数目相等,改变压强不影响平衡移动;
C.化学反应速率之比等于其化学计量数之比;
D.利用速率之比等于化学计量数之比计算.
解答 解:A.化学反应速率是单位时间内的平均速率,不是瞬时速率,5min时,测得C为xmol,5min内平均速率v(C)=$\frac{\frac{xmol}{VL}}{300s}$=$\frac{x}{300V}$mol/(L.min),故A错误;
B.不能确定反应前后气体的分子数目是否变化,若反应气体气体分子数目相等,改变压强不影响平衡移动,故B错误;
C.化学反应速率之比等于其化学计量数之比,则0-5min内v(A):v(C)=a:c,故C正确;
D.速率之比等于化学计量数之比,则v(A)=$\frac{a}{c}$×v(C)=$\frac{a}{c}$×$\frac{x}{300V}$mol/(L.min)=$\frac{ax}{300cV}$mol/(L.min),故D错误.
故选:C.
点评 本题考查化学反应速率有关计算,常利用速率定义式与速率规律进行计算,注意化学反应速率表示单位时间内浓度变化量,为一段时间内平均速率.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
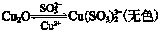
| 操作 | 现象 |
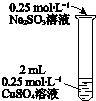 | i 有黄色沉淀出现,随着 Na2SO3溶液的滴入,沉淀增加,当加到5mL时,溶液的蓝色消失. ii 将试管加热,黄色沉淀变为砖红色,有刺激性气味气体产生. iii在加热条件下,继续滴入Na2SO3溶液,砖红色沉淀减少,当1加到10mL时,沉淀完全溶解,得无色溶液. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
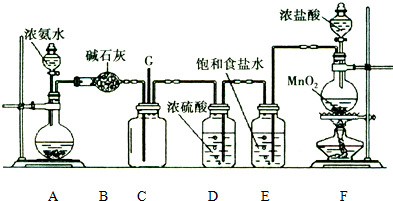
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
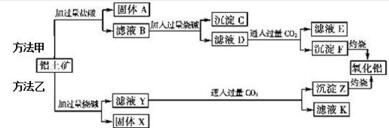
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 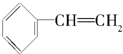 | B. | 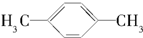 | C. | 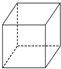 | D. | 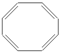 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能发生丁达尔现象 | |
| B. | 胶体粒子能通过滤纸空隙 | |
| C. | 胶体在一定条件下能稳定存在 | |
| D. | 胶体分散质粒子直径在1nm~100nm之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ba2+、CO32-、NO3- | B. | Na+、OH-、K+、MnO4- | ||
| C. | K+、HCO3-、SO42-、Na+ | D. | H+、Cl-、Cu2+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18g冰晶体中含有氢键的数目为2NA | |
| B. | 1molH2O2中含有非极性键的数目为NA | |
| C. | 1molSiO2晶体中含有Si-O键的数目为4NA | |
| D. | 22.4LHF(标准状况)中含有氟原子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池的负极锌发生还原反应 | |
| B. | 该电池反应中二氧化锰起催化剂作用 | |
| C. | 当0.lmol Zn完全溶解时,流经电解液的电子个数约为1.204×1023 | |
| D. | 电池正极反应式为 MnO2+e-+H20═MnO(OH)+OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com