
���� ��1����Ӧ8Al+3Fe3O4 $\frac{\underline{\;����\;}}{\;}$4Al2O3+9Fe�У�AlԪ�ػ��ϼ����ߣ���������Ϊ��ԭ����FeԪ�ػ��ϼ۽��ͣ�����ԭ��Al2O3Ϊ���������ɴ˷������
��2�����������ܹ���ˮ��������̼��Ӧ����������̼���������ȷֽ�����̼���ơ�ˮ�Ͷ�����̼��
��3���������ӵ���Һ�еμ�KSCN��Һ����Һ��ΪѪ��ɫ��
��� �⣺��1��8Al+3Fe3O4 $\frac{\underline{\;����\;}}{\;}$4Al2O3+9Fe�Ƿ��ȷ�Ӧ��AlԪ�ػ��ϼ����ߣ���������Ϊ��ԭ�����ʴ�Ϊ�����ȣ�Al��
��2�����������ܹ���ˮ��������̼��Ӧ������������2Na2O2+2CO2=2Na2CO3+O2������ΪDZˮͧ�ͺ��������������Դ��̼���������ȷֽ�����̼���ơ�ˮ�Ͷ�����̼���ܹ������ᷴӦ�����ڱ��Ƹ�㣬Ҳ����������ҩ���ʴ�Ϊ��Na2O2��NaHCO3��
��3���������ӵ���Һ�еμ�KSCN��Һ����Һ��ΪѪ��ɫ���ʴ�Ϊ���죮
���� ���⿼����������ԭ�����֪ʶ�����ʵ���;����Ϥ���ʵ������ǽ���ؼ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Kp=$\frac{P��N{H}_{3}��^{4}��P��{O}_{2}��^{5}}{P��NO��^{4}��P��{H}_{2}O��^{6}}$ | |
| B�� | �����¶ȣ���Kp������÷�ӦΪ���ȷ�Ӧ | |
| C�� | �÷�Ӧ�ﵽƽ��״̬������ѹǿ��ƽ�������ƶ���Kp��С | |
| D�� | 2NH3��g��+$\frac{5}{2}$O2��g��?2NO��g��+3H2O��g�� ��ƽ�ⳣ��Kp=��$\frac{1}{2}$��a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�11.2L H2��D2�Ļ��������������������ΪNA | |
| B�� | ������ˮ��ͨ��1mol��������Ӧ��ת�Ƶĵ�����ΪNA | |
| C�� | 28g��ϩ�ͱ�ϩ�Ļ����������̼̼˫������ĿΪNA | |
| D�� | 1L0.5mol•L-1Na2CO3��Һ�������ӵ�����Ϊ0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
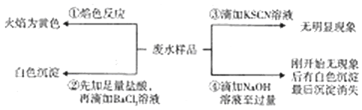
| A�� | ��ˮ����Na+������K+ | B�� | ��ˮ����SO42-��CO32- | ||
| C�� | ��ˮ����Fe3+�����ܺ�Fe2+ | D�� | ��ˮһ������Na+��Al3+��SO42-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
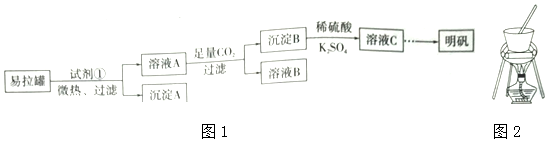
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
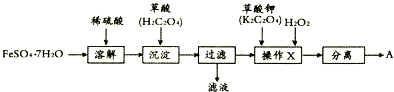
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij��ѧ����ʵ��С�������ͼʾʵ��װ������ȡ�屽��֤���÷�ӦΪȡ����Ӧ����֪���屽���۵�Ϊ?30.8�棬�е�156�森
ij��ѧ����ʵ��С�������ͼʾʵ��װ������ȡ�屽��֤���÷�ӦΪȡ����Ӧ����֪���屽���۵�Ϊ?30.8�棬�е�156�森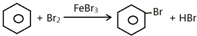 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
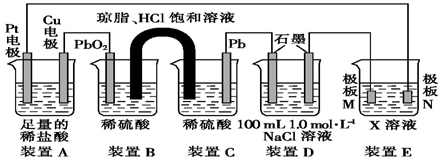
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ����Ļ�ѧʽ | CH3COOH | HCN | H2CO3 |
| ����ƽ�ⳣ�� | 1.8��10-5 | 4.9��l0-10 | K1=4.3��10-7����K2=5.6��10-11 |
| A�� | �����������μ�ˮ������ĵ���Ⱥ�pH��������С | |
| B�� | �����ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH��NaCN����pH��Na2CO3����pH��CH3COONa�� | |
| C�� | 25��ʱ����CH3COOH��Һ��NaCN��Һ�У�ˮ�ĵ���̶�ǰ�ߴ� | |
| D�� | amol•L-1HCN��Һ��bmol•L-1NaOH��Һ�������ϣ�������Һ��c��Na+����c��CN-������bһ��С��a |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com