
| A. | 二氧化三碳的电子式为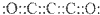 | B. | C3O2、CO、CO2都是碳的氧化物 | ||
| C. | C3O2和CO一样可以燃烧生成CO2 | D. | C3O2和CO2都是碳酸的酸酐 |
分析 A、二氧化三碳中所有原子最外层均达到8电子稳定结构,则其结构式为:O=C=C=C=O;
B、氧化物是由两种元素构成,其中一种是氧元素的化合物;
C、根据C3O2和CO中碳元素的化合价分析;
D、碳酸中碳元素的化合价为+4价,根据碳元素的化合价分析.
解答 解:A、二氧化三碳中所有原子最外层均达到8电子稳定结构,则其结构式为:O=C=C=C=O,其电子式为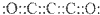 ,故A正确;
,故A正确;
B、氧化物是由两种元素构成,其中一种是氧元素的化合物,所以C3O2、CO、CO2都是碳的氧化物,故B正确;
C、C3O2中碳元素的化合价为+3价和CO中碳元素的化合价为+2价,碳元素充分燃烧的产物是二氧化碳,其中碳元素的化合价为+4价,所以C3O2和CO一样可以燃烧生成CO2,故C正确;
D、碳酸中碳元素的化合价为+4价,其酸酐为二氧化碳,而C3O2中碳元素的化合价为+3价,所以它不是碳酸的酸酐,故D错误;
故选D.
点评 本题考查了碳的氧化物,主要考查了电子式、氧化物的概念、酸酐等,难度中等,注意把握电子式的书写方法.


科目:高中化学 来源: 题型:解答题
| 浓度 时间(s) 反应条件 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热(t1℃) | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热(t2℃) | 360(a) | 480 | 540 | 720 |
| MnO2催化剂、加热(t2℃) | 10(b) | 25 | 60 | 120 |
| 催化剂(MnO2) | 操作情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 | 3min |
| 块状 | 反应较慢,火星红亮但木条未复燃 | 30min |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C14H18O5 | B. | C14H16O4 | C. | C16H22O5 | D. | C16H20O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
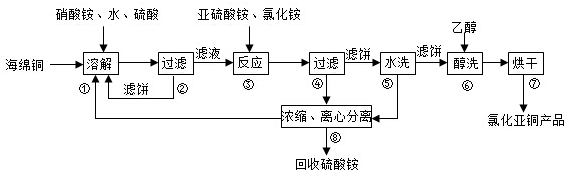
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于水中存在氢键,所以水很稳定 | |
| B. | 能与酸反应生成盐和水的氧化物一定是碱性氧化物 | |
| C. | Na2O2中既含有离子键,又含有非极性键 | |
| D. | 由于C═O键是极性键,所以CO2是极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该溶液c(H+)≥0.1 mol/L | |
| B. | 把该溶液稀释成1 L后,pH≥2 | |
| C. | 把该溶液稀释成1 L后,pH≤2 | |
| D. | 中和此溶液需0.1mol/L的NaOH体积≥100mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com