
下列物质的转化在给定条件下能一步实现的是( )
①NaAlO2(aq)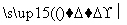 AlCl3
AlCl3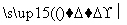 Al
Al
②NH3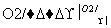 NO
NO HNO3
HNO3
③NaCl(饱和)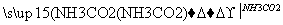 NaHCO3
NaHCO3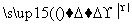 Na2CO3
Na2CO3
④FeS2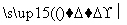 SO3
SO3 H2SO4
H2SO4
A.②③ B.①④
C.②④ D.③④
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
下列离子方程式中正确的是
A.硫化亚铁放入盐酸中 S2-+2H+=H2S↑
B.硫酸铜溶液中通入硫化氢Cu2++ H2S=CuS↓+2 H+
C.氢氧化钠溶液中通入过量CO2 2OH-+CO2=CO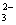 +H2O
+H2O
D.碳酸氢铵溶液中加入过量氢氧化钠溶液HCO + OH-= CO
+ OH-= CO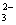 +H2O
+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁由H+、Na+、Al3+、Ba2+、OH-、Cl-、HCO 中的两种组成,可以发生如图转化,下列说法正确的是( )
中的两种组成,可以发生如图转化,下列说法正确的是( )
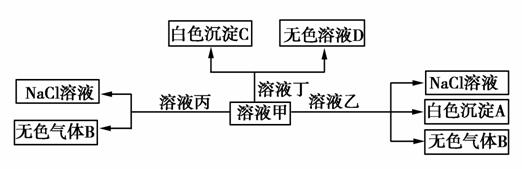
A.甲为AlCl3,乙为NaHCO3
B.溶液丙中还可以大量共存的离子有Fe2+、NO 、SO
、SO
C.在甲中滴加丁开始反应的离子方程式:HCO +Ba2++OH-===BaCO3↓+H2O
+Ba2++OH-===BaCO3↓+H2O
D.白色沉淀A可能溶解在溶液D中
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室合成环己酮的反应、装置示意图及有关数据如下:


环己醇、环己酮、饱和食盐水和水的部分物理性质见下表
| 物质 | 沸点(℃) | 密度 (g·cm-3,20 ℃) | 溶解性 |
| 环己醇 | 161.1(97.8) | 0.962 4 | 能溶于水 |
| 环己酮 | 155.6(95) | 0.947 8 | 微溶于水 |
| 饱和食盐水 | 108.0 | 1.330 1 | |
| 水 | 100.0 | 0.998 2 |
注:括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
(1)酸性Na2Cr2O7溶液氧化环己醇反应的ΔH<0,反应剧烈将导致体系温度迅速上升,副反应增多。实验中通过装置B将酸性Na2Cr2O7溶液加到盛有环己醇的A中,在55~60 ℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100 ℃的馏分,得到主要含环己酮粗品和水的混合物。
①如何滴加酸性Na2Cr2O7溶液____________________,用漂粉精和冰醋酸代替酸性Na2Cr2O7溶液也可氧化环己醇制环己酮,用漂粉精和冰醋酸氧化突出的优点是__________________。
②蒸馏不能分离环己酮和水的原因是___________________。
(2)环己酮的提纯需要经过以下一系列的操作:a.蒸馏,收集151~156 ℃馏分,b.过滤,c.在收集到的馏分中加NaCl固体至饱和,静置,分液,d.加入无水MgSO4固体,除去有机物中少量水。
①上述操作的正确顺序是________(填字母)。
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有________。
③在上述操作c中,加入NaCl固体的作用是________。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有________种不同化学环境的氢原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示装置进行实验,下列对实验现象的解释不合理的是( )
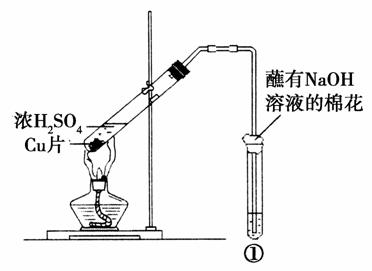
| 选项 | ①中试剂 | ①中现象 | 解释 |
| A | Ba(NO3)2溶液 | 生成白色沉淀 | SO |
| B | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
| C | 紫色石蕊溶液 | 溶液变红 | SO2与水反应生成酸 |
| D | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的应用与性质相对应的是( )
A.氢氟酸可用于雕刻玻璃是因为其具有酸性
B.SO2可用作漂白剂是因为其具有还原性
C.浓硫酸可用作干燥剂是因为其具有强氧化性
D.氯化铁溶液可用于制作印刷电路板是因为其能氧化铜
查看答案和解析>>
科目:高中化学 来源: 题型:
用石墨电极电解100 mL H2SO4与CuSO4的混合溶液,通电一段时间后,两极均收集到2.24 L气体(标准状况),则原混合溶液中Cu2+的物质的量浓度为( )
A.1 mol·L-1 B.2 mol·L-1C.3 mol·L-1 D.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理
B.用pH计、电导率仪(一种测量溶液导电能力的仪器)均可检测乙酸乙酯的水解程度
C.邻苯二甲酸氢钾可用于标定NaOH溶液的浓度,假如称量邻苯二甲酸氢钾时电子天平读数比实际质量偏大,则测得的NaOH溶液浓度比实际浓度偏小
D.向某溶液中加入茚三酮试剂,加热煮沸后溶液若出现蓝色,则可判断该溶液含有蛋白质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com