
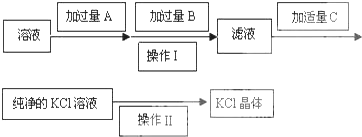
分析 为了除去KCl溶液中少量的MgCl2、MgSO4,由流程可知,加过量A为Ba(OH)2,发生MgCl2+Ba(OH)2═BaCl2+Mg(OH)2↓、MgSO4+Ba(OH)2═BaSO4↓+Mg(OH)2↓,再加B为K2CO3,K2CO3在Ba(OH)2之后可将过量钡离子除去,操作I为过滤,滤液中含KCl及过量的K2CO3,适量C为HCl,反应后得到KCl溶液,操作II为蒸发结晶,得到KCl晶体,以此来解答.
解答 解:为了除去KCl溶液中少量的MgCl2、MgSO4,由流程可知,加过量A为Ba(OH)2,再加B为K2CO3,K2CO3在Ba(OH)2之后可将过量钡离子除去,操作I为过滤,滤液中含KCl及过量的K2CO3,适量C为HCl,反应后得到KCl溶液,操作II为蒸发结晶,得到KCl晶体,
(1)氢氧化钡可以将MgCl2、MgSO4中的氢氧根和硫酸根除去,除杂时,每一步所加的试剂均是过量的,过量的氢氧化钡需用碳酸钾除去,而多余的碳酸钾需用盐酸来除去,故试剂A、B、C依次是Ba(OH)2、K2CO3、HCl,
故答案为:Ba(OH)2;K2CO3;HCl;
(2)操作I为液体和固体分离的方法是过滤,所用玻璃仪器有漏斗、玻璃棒、烧杯,故答案为:过滤;
(3)加过量B的目的是使溶液中的Ba2+完全沉淀,故答案为:使溶液中的Ba2+完全沉淀;
(4)碳酸根的特征离子反应:与强酸生成气体二氧化碳,与BaCl2溶液、CaCl2溶液反应生成沉淀,则检验B是否过量的方法是检验B是否过量的方法是去滤液少许于试管中,向试管中滴加稀盐酸,若有气泡产生,说明:K2CO3过量,故答案为:检验B是否过量的方法是去滤液少许于试管中,向试管中滴加稀盐酸,若有气泡产生,说明:K2CO3过量.
点评 本题考查混合物分离提纯综合应用,为高频考点,把握流程中的反应及混合物分离提纯方法为解答的关键,侧重分析与应用能力的考查,注意试剂的先后顺序,题目难度不大.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:选择题
| A. | 用热的碱水清除炊具上残留的油污比冷的碱水清除效果好 | |
| B. | 面粉和炒菜用的花生油的主要成分均为天然高分子化合物 | |
| C. | 炒菜用过的铁锅,经放置常出现红棕色斑迹,主要发生的是电化学腐蚀 | |
| D. | 早餐经常食用的豆浆和牛奶均属于胶体,且均含有丰富的蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙溶于醋酸CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 澄清石灰水中加入盐酸Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 铜片加入稀硝酸中3Cu+2NO3-+8H+═3Cu2++2N0↑+4H20 | |
| D. | 小苏打溶液和盐酸混合CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
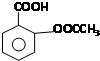 阿司匹林(Aspirin)也叫乙酰水杨酸(结构如图所示)是一种历史悠久的解热镇痛药.下列有关说法正确的是( )
阿司匹林(Aspirin)也叫乙酰水杨酸(结构如图所示)是一种历史悠久的解热镇痛药.下列有关说法正确的是( )| A. | 与乙酰水杨酸具有相同官能团的芳香族同分异构体共有8种(不考虑立体异构) | |
| B. | 乙酰水杨酸的所有原子均在同一平面上 | |
| C. | 乙酰水杨酸能发生取代、加成、氧化、还原反应 | |
| D. | 乙酰水杨酸易溶于水、乙醇等溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将pH=3 的①溶液与pH=11的②溶液等体积混合,溶液pH>7 | |
| B. | 若三种溶液浓度相同,将溶液①、②等体积混合,混合液中c(CH3COO-)等于溶液③中的c(CH3COO-) | |
| C. | 将①、②等浓度体积混合,混合液中c(CH3COO-)+c(CH3COOH)═c(Na+) | |
| D. | 若②、③的pH值相同,则两种溶液中水的电离程度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当有10NA个电子转移时,该反应放出1300kJ的能量 | |
| B. | 当有10NA个碳氧共用电子对生成时,放出1300kJ的能量 | |
| C. | 当有2NA个碳氧共用电子对生成时,放出1300kJ的能量 | |
| D. | 当有1NA个水分子生成且为液体时,吸收1300kJ的能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com