
| A、氧化钙用作儿童食品的干燥剂存在安全隐患 |
| B、聚乙烯、聚氯乙烯、聚苯乙烯都是通过加聚反应制得的 |
| C、雾霾天气对人的健康造成危害,“雾”和“霾”的分散质微粒不相同 |
| D、绿色化学的核心是利用化学原理对环境污染进行治理 |


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
| A、1.0mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B、甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- |
| C、与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
| D、c(H+)/c(OH-)=1×10-13的溶液K+、Na+、CH3COO-,Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
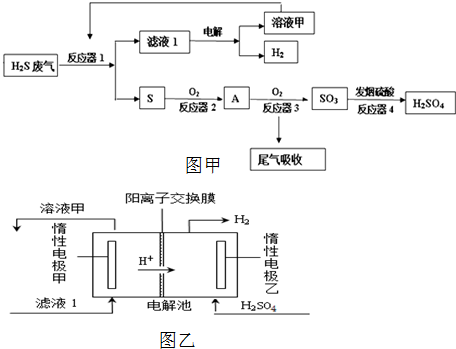
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作 | 实验现象 | 结论 | |
| A | 向某溶液中加入氯化钡、稀硝酸的混合液 | 产生白色沉淀 | 该溶液中一定含有SO42-或SO32- |
| B | 将某气体通入品红溶液 | 溶液红色褪去 | 该气体一定SO2 |
| C | 把湿润的碘化钾--淀粉试纸放入某一红棕色的气体中 | 试纸变蓝色 | 该气体可能是NO2 |
| D | 将通入SO2到酸性高锰酸钾溶液中 | 溶液紫色褪去 | SO2具有漂白性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
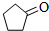 )可由环戊烷经三步反应合成:
)可由环戊烷经三步反应合成: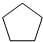
| 反应1 |
| 反应2 |
| 反应3 |
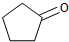
| A、反应1可用试剂是氯气 |
| B、反应3可用的试剂是氧气和铜 |
| C、反应1为取代反应,反应2为消去反应 |
| D、A可通过加成反应合成Y |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| Cu的平均溶解速率(×10-3mol.min-1 | 7.34 | 3.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3COOH与HCN均为弱酸,酸性:HCN>CH3COOH |
| B、25℃时,水电离出来的c(H+)均为 10-11mol/L的两种酸,酸的浓度:HCN>CH3COOH |
| C、25℃时,浓度均为0.1 mol/L 的CH3COONa和NaCN溶液中,pH大小:CH3COONa>NaCN |
| D、25℃时,pH均为3的CH3COOH与HCN溶液各100ml与等浓度的NaOH溶液反应,消耗NaOH溶液体积:CH3COOH>HCN |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、沸点:NH3>PH3>AsH3 |
| B、结合质子的能力:OH->CH3COO->Cl- |
| C、酸性:HClO4>H2SO4>H3PO4 |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com