
【题目】合金是一类用途广泛的金属材料,下列关于合金的描述正确的是( )
A.合金的硬度比组成它的成分金属小
B.在我国,使用最早的合金是青铜
C.合金的熔点一般比组成它的成分金属高
D.目前用量最大、用途最广的合金是铝合金
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
【题目】每到冬天就会出现大雾天气,能见度不到10米,致使汽车行驶受阻,下列关于雾的说法正确的是( )
A.无法确定雾中水滴的直径大小
B.不会产生丁达尔现象
C.雾中水滴的直径在1nm~100nm间
D.雾中水滴的直径小于1nm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分:
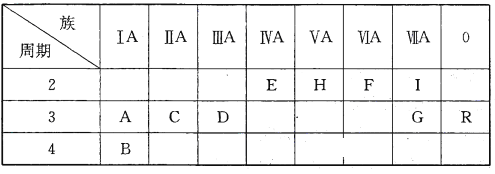
根据要求回答下列问题:
(1)十种元素中化学性质最不活泼的元素是__________________(填元素符号,下同),形成化合物种类最多的元素是_____________________。
(2)A、C、D三种元素的最高价氧化物对应的水化物,其中碱性最强的是______________(填化学式,下同),E、H、G三种元素的最高价氧化物对应的水化物中酸性最强的是______________。
(3)I元素跟A元素形成化合物的电子式是______________。高温灼烧该化合物时,火焰呈______________色。
(4)分别写出B、G两种单质和水反应的离子方程式_____________、________________。
(5)元素A和F能形成两种化合物,写出其中较稳定的化合物与CO2反应生成氧气的化学方程式:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要配制0.50 mol·L—1 NaCl溶液480 mL。按下列操作步骤填上适当的文字,使整个操作完整。
(1)选择仪器。完成本实验必须用到的仪器有:托盘天平(带砝码,最小砝码为5g)、量筒、药匙、烧杯、玻璃棒、____________、____________以及等质量的两片滤纸。
(2)计算。配制该溶液需取NaCl晶体____________g。
(3)称量。
①天平调平之后,应将天平的游码调至某个位置,请在下图中用一根竖线标出游码左边缘所处的位置:
![]()
②称量过程中NaCl品体应放于天平的____________(填“左盘”或“右盘”)。
③称量完毕,将药品倒人烧杯中。
(4)溶解、冷却。该步实验中需要使用玻璃棒,目的是________________________。
(5)移液、洗涤。在移液时应使用________________________引流,需要洗涤烧杯2~3次是为了____________________________________。
(6)定容。向容量瓶中加水至液面接近刻度线____________处,改用____________加水,使溶液凹液面与刻度线相切。
(7)摇匀、装瓶。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100 mL稀H2SO4溶液;以0.14mol/L的NaOH溶液滴定上述稀H2SO425mL,滴定终止时消耗NaOH溶液15mL。
(1)该学生用标准0.14 mol/L NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25 mL,注入锥形瓶中,加入指示剂。
B.用待测定的溶液润洗酸式滴定管。
C.用蒸馏水洗干净滴定管。
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。
E.检查滴定管是否漏水。
F.另取锥形瓶,再重复操作一次。
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是(用序号填写):_______________。
②该滴定操作中应选用的指示剂是:____________________。
③在G操作中如何确定终点?__________________________________。
(2)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰好合适”)________,原因是__________________________。
(3)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度__________mol/L(保留二位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,将1.0Lcmol·L-1CH3COOH 溶液与0.1molNaOH 固体混合,使之充分反应。然后向该混合溶液中通入HCl或加入NaOH 固体(忽略体积和温度变化),溶液pH随通入(或加入) 物质的量的变化如右图所示。下列叙述正确的是( )

A. 水的电离程度: a>b>c
B. c 点对应的混合溶液中,c(CH3COOH)>c(Na+ )>c(OH-)
C. a 点对应的混合溶液中,c(Na+ )=c(CH3COO-)
D. 该温度下,醋酸的电离平衡常数Ka=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以Na2SO3粉末和70%H2SO4为原料制取SO2, 且以SO2为原料制取物质和进行性质探究。回答下列问题:
(1)学生甲欲收集一瓶干燥的SO2,选择图中的装置,其连接顺序为_________ (按气流方向,用小写字母表示); SO2有毒,为防止中毒实验应在_________中进行。

(2)学生乙欲通过量气法测定在空气中久置的亚硫酸钠粉末的纯度,最好选择下列装置 中 的_________(填字母) 。

(3)学生丙欲以CuSO4·5H2O 和SO2 等为原料制备谢弗勒尔盐(Cu2SO3·CuSO3·2H2O)实验装置如右图所示。已知谢弗勒尔盐是一种深红色固体,不溶于水和乙醇,100℃时发生分解。

回答下列问题:
装置A中SO2的作用是___________________; 体 系 温度 控 制 在 60~80℃ 的目的是___________。装置B的作用是_________。
(4)学生丁欲利用右图装置探究SO2使品红溶液褪色的实质。实验中观察到Ⅰ中红色褪去;Ⅱ中无现象。据此推断能使品红水溶液褪色的粒子可能是_________。如果要比较这些粒子使品红溶液褪色的快慢,请设计实验方案,简述操作和需要观察的现象________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对图两种化合物的结构或性质描述正确的是:

A. 均能与溴水反应 B. 分子中肯定共平面的碳原子数相同
C. 不是同分异构体 D. 可以用红外光谱区分,但不能用核磁共振氢谱区分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,室温下向盛有3.0 mL NO的试管中缓缓通入1.5 mL O2(所有气体体积均在标准状况下测定)。

试回答下列问题:
(1)写出观察到的现象(可不写满,也可补充):
①___________;
②___________;
③___________。
(2)最终试管中剩余的气体是______,体积为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com