
| A. | 制半导体材料的元素 | B. | 制农药的元素 | ||
| C. | 制催化剂的元素 | D. | 制耐高温合金的元素 |
分析 A、制半导体的材料在金属和非金属的分界线附近找;
B、新制农药元素可以从周期表的非金属元素中找;
C、制造催化剂的材料在过渡元素区找;
D、制耐高温合金元素在元素周期表的过渡金属中能找到.
解答 解:A.位于元素周期表中金属和非金属元素的分界线的附近的元素既有金属性又有非金属性,则制半导体的材料在金属和非金属的分界线附近找,故A不选;
B.新制农药元素可以从周期表的左上角中的非金属元素中找到,故B不选;
C.制造催化剂的材料在过渡元素区找,如铁或钒等,故C选;
D.制耐高温合金元素在元素周期表的过渡金属中能找到,故D选.
故选CD.
点评 本题考查元素周期表与元素的性质知识,题目较为简单,熟悉元素在周期表中的位置及性质即可解答.


科目:高中化学 来源: 题型:选择题
| A. | 加入少量W,逆反应速率增大,平衡左移 | |
| B. | 加压,正反应速率增大,逆反应速率减小 | |
| C. | 温度、体积不变,充入He气加压,反应速率加快 | |
| D. | 升温,混合气平均相对分子质量减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采用电解水法制取无污染的氢能 | B. | 完善煤液化制取汽油的技术 | ||
| C. | 研制推广以甲醇为燃料的汽车 | D. | 进一步提高石油加工工艺 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
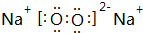 .
. ,空间构型直线型,属于非极性分子(填“极性”或“非极性”)
,空间构型直线型,属于非极性分子(填“极性”或“非极性”)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
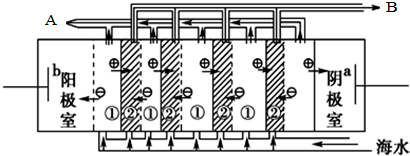
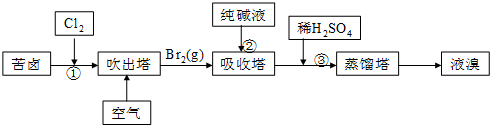
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4 | B. | C2H5OH | C. | 稀HNO3 | D. | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
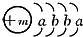 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com