
| A、H2O2的氧化性比Fe3+强,其还原性比Fe2+弱 |
| B、在H2O2分解过程中,溶液的酸碱性不变 |
| C、在H2O2分解过程中,Fe2+和Fe3+的总量保持不变 |
| D、H2O2生产过程要严格避免混入Fe2+ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
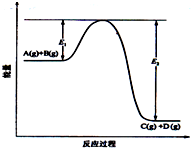 反应A(g)+B(g) 错误!未找到引用源C(g)+D(g)过程中的能量变化如图所示,请回答下列问题:
反应A(g)+B(g) 错误!未找到引用源C(g)+D(g)过程中的能量变化如图所示,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
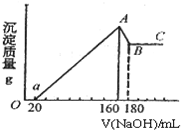 将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.
将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④③②① | B、①④③② |
| C、②③④① | D、①④②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C |
| B、C和S |
| C、KNO3 |
| D、S和KNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 L 1.2 mol?L-1的NaCl溶液 |
| B、2 L 1 mol?L-1的NaOH溶液 |
| C、0.5 L 0.8 mol?L-1的Na2SO4溶液 |
| D、3 L 0.5 mol?L-1的Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸的强弱:HCN>HClO |
| B、pH:HClO>HCN |
| C、与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN |
| D、酸根离子浓度:c(CN-)<c(ClO-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com